įl≤ľ»’∆ŕ£ļ2025-9-17 10:54:19
1°Ę“ż—‘
‚Ā“Ú∆šŃľļ√Ķń…ķőÔŌŗ»›–‘°ĘńÕłĮőg–‘°ĘĶÕ√‹∂»“—◊ųěť—ņ∑N÷≤ůwŹV∑ļ”√”ŕŐśīķ»Ī ßĶń—ņżX£¨Ti6Al4V“Ú∆šłŁļ√ĶńôC–Ķ–‘ń‹“≤ «ľÉ‚ĀĶńņŪŌŽŐśīķ∆∑[1]°£ĆćŽHĎ™”√÷–—ņ∑N÷≤ůw÷‹áķĶńĻ«ĹMŅóÕ®Ŗ^Ļ«÷ōň‹ĀŪŖmĎ™ôC–Ķōďļ…[2]°£»Ľ∂Ý£¨‚Āľį∆šļŌĹū£®110GPa£©ĶńŹó–‘ń£ŃŅŌŗĪ»”ŕĻ«ųņ£®10~30GPa£©Ŗ^łŖ£¨Źń∂ÝĆß÷¬ĹūĆŔ÷≤»ŽőÔļÕĻ«ĹMŅóťgĶń“ϙѶ∆ŃĪő”–ßĎ™£¨ŖM∂Ý“żįlĻ«ĹYļŌ≤ĽŃľļÕ÷≤»ŽőÔň…Ą”[3]°£īňÕ‚£¨Ti6Al4V‘ŕŅŕ«Ľ∑N÷≤ļůēĢŠĆ∑Ň”–∂ĺĶńAlļÕVĹūĆŔŽx◊”£¨ő£ļ¶»ňůwĹ°ŅĶ[4–5]°£“Úīň£¨šÜļŌĹū“Ú∆šÉěģźĶńńÕłĮőg–‘°ĘŃľļ√ĶńѶĆW–‘ń‹°Ę‘ŕůwÉ»Ņ…–ő≥…Ļ«†ÓŃ◊Ľ“ ĮĆ”“‘ľįĺŖ”–›^ĶÕīŇĽĮ¬ £¨◊ųěťĻ«Ņ∆÷≤»ŽŐśīķ≤ńŃŌ ‹ĶĹ‘ĹĀŪ‘Ĺ∂ŗĶńÍP◊Ę[6]°£ńŅ«įƶ÷≤»ŽšÜļŌĹūĶń—–ĺŅ÷ų“™áķņ@ŐŪľ”βŌŗ∑Ä∂®‘™ňō“‘ę@Ķ√Źó–‘ń£ŃŅłŁĶÕĶńļ¨βŌŗšÜļŌĹū£¨—–ĺŅ›^읏V∑ļĶńŠt”√šÜļŌĹūįŁņ®Zr-TiŌĶľįZr-NbŌĶ[7–9]°£Ć¶”ŕZrTiŌĶļŌĹū£¨ZrļÕTi2∑N‘™ňōĆŔ”ŕÕ¨“Ľ÷ų◊Ś£¨ĺŖ”–Ōŗň∆ĶńőÔņŪĽĮĆW–‘Ŕ|ļÕĺßůwĹYėč£¨≤Ę«“Ņ…“‘–ő≥…üoŌřĻŐ»‹ůw£¨ ģ∑÷Ī„”ŕŖM––ļŌĹū≥…∑÷‘O”č°£HsuĶ»»ň[10]ƶĪ»ŃňŤTĎBZr-xTi£®x=10,20,30,40,wt%£©ļŌĹūĶńѶĆW–‘ń‹£¨įl¨FZr-TiļŌĹū≤ĽÉHŅĻŹĚŹä∂»łŖ”ŕľÉšÜ£¨ŖÄĺŖ”–Ńľļ√Ķń—”’Ļ–‘£ĽŹó–‘ń£ŃŅ ∑∂áķ‘ŕ68GPa£®Zr-30Ti£©÷Ń78GPa£®Zr-40Ti£©£¨Ô@÷ÝĶÕ”ŕľÉ‚Ā£¨”–ÕŻ≥…ěť–¬–ÕŅŕ«Ľ∑N÷≤≤ńŃŌ°£ģĒZrļÕTiĶń‘≠◊”Ī»Ĺ”ĹŁ1:1ēr£®Zr-30wt%Ti£©£¨ĻŐ»‹ŹäĽĮĶń–ßĻŻ◊Óīů[11]°£Ć¶”ŕZr-NbŌĶļŌĹū£¨ZrļÕNb «Õ¨“Ľ÷‹∆ŕŌŗŗŹ‘™ňō£¨β-NbļÕβ-ZrĺßůwĹYėčŌŗÕ¨£¨ŁcÍáÖĘĒĶļÕ‘≠◊”įŽŹĹŌŗĹŁ£¨“ÚīňZr-NbļŌĹūĶńŁcÍἯ◊É–°£¨ŌŗĎ™ĶōŹó–‘ń£ŃŅ›^∆šňŻůwŌĶłŁĶÕ°£
Nb «šÜļŌĹū◊Ó≥£”√ĶńβŌŗ∑Ä∂®‘™ňō£¨ģĒNbļ¨ŃŅīů”ŕ22wt%ērļŌĹūŅ…”…Üő“ĽβŌŗĹM≥…£¨ľśĺŖ›^ĶÕĶńŹó–‘ń£ŃŅļÕłŖ—”’Ļ–‘ľįŖm∂»ĶńŹä∂»[12]°£ĪMĻ‹“—”–›^∂ŗƶ”ŕ–¬–ÕŠt”√šÜļŌĹū◊ųěťĻ«Ņ∆ļÕ—ņŅ∆≤ńŃŌĶń—–ĺŅ£¨≤ĘŖM––ŃňŌŗÍPĶńůwÕ‚úy‘á[6,13]£¨ĶęĺŗŽx’ś’żĶńŇRī≤Ď™”√ŖÄ–Ť“™łŁ…Ó»ŽĶń—–ĺŅļÕĆŹ≤ť°£
”…”ŕÕ‚≤Ņ›dļ…–ő≥…ĶńϙѶϙ◊ÉŅō÷∆÷Ý»ňůwĻ«ĹMŅóĶńѶĆWŪĎĎ™£¨…ķőÔѶĆWĶń”įŪĎƶ”ŕÓAúy≥…Ļ¶÷≤»ŽĺŖ”–÷ō“™◊ų”√°£ŇRī≤Ď™”√÷–£¨÷≤»ŽőÔ√śŇRŹÕŽsĶń…ķőÔѶĆWÜĖÓ}£¨∂Ý≤…”√ŹÕŽsĶńĽÓůwĆćÚěļ‹Žy»•ŃňĹ‚…ķőÔѶĆWŖ^≥Ő[14]°£Ą”őÔ—–ĺŅŅ…“‘÷ĪĹ””^≤žĶĹĻ«ĹMŅóƶ∑N÷≤ůw÷≤»ŽļůĶńϙѶĪŪ¨F≥ŲĶń…ķőÔѶĆW∑īĎ™£¨Ķęļ‹Žy‘uĻņÉ»≤ŅĶńϙѶϙ◊É°£ĪMĻ‹“Ľ–©ĆćÚěĶń∑Ĺ∑®£¨»ÁĎ™◊ÉÉx£¨Ņ…“‘ĺęī_Ņō÷∆›dļ…Ķńīů–°ĀŪ‘uĻņĪŪ√śĎ™◊É£¨Ķęüo∑®‘uĻņĎ™◊ÉÉx÷ģÕ‚ĶńÖ^”Ú[15]°£“Ú”–Ōř‘™∑Ĺ∑® «ń£ĒMļÍľö”^≤ńŃŌѶĆW–‘ń‹—›ĽĮĶń”––ß∑Ĺ∑®£¨‘ŕ…ķőÔŠtĆWÓI”Ú”–÷ÝŹV∑ļĶńĎ™”√[16–17]°£”–Ōř‘™◊ųěť“Ľ∑NĒĶ÷Ķń£ĒM∑Ĺ∑®£¨‘ ‘S—–ĺŅ’Ŗ‘ŕŖM––ůwÉ»ĆćÚě÷ģ«įƶňý—–ĺŅĶńÜĖÓ}ŖM––≥ű≤Ĺ‘uĻņ£¨Ņ…”√”ŕ”^≤ž∑N÷≤ůwľįĻ«ĹMŅóĶńϙѶϙ◊É∑÷≤ľľįľöĻĚ£¨Źń∂Ý—–ĺŅ∑N÷≤ůw≤ńŃŌĶń…ķőÔѶĆW–‘ń‹£¨ÓAúyĻ«ĹMŅóĶń…ķőÔѶĆW––ěť°£‘ŕĆć¨F—–ĺŅŌÚŇRī≤Ď™”√řDĽĮĶń¬ĢťLŖ^≥Ő÷–£¨”–Ōř‘™∑Ĺ∑®ľ”ňŔŃňŖM≥Ő≤ĘŐŠĻ©…Ó»Žľö÷¬Ķń—–ĺŅĹYĻŻľį“鬅°£“Úīň£¨”–Ōř‘™∑÷őŲ‘ŕ—ņŅ∆≤ńŃŌĶńŖxďŮ÷–∆ūĶĹ÷ō“™◊ų”√£¨≤Ę«“‘ŕ∆šňŻ–¬–ÕŐśīķ≤ńŃŌ£®»ÁPEEK°Ę—űĽĮšÜ£©Ķń…ķőÔѶĆW–‘ń‹—–ĺŅĶ√ĶĹ›^∂ŗĶńĎ™”√[17–19]°£»Ľ∂Ý£¨‘ŕ∑N÷≤—ņĶń…ķőÔѶĆW––ěť—–ĺŅ÷–£¨…ķőÔůwĶńŹÕŽs–‘ļÕĄ”ĎB–‘ ĻĶ√ Ļ”√”čň„ôCüo∑®ÕÍ»ęŹÕ÷∆√ŅāÄľöĻĚ[20]°£“Úīň≤…”√žoĎBľ”›dĶń∑Ĺ Ĺƶ÷≤»ŽőÔļÕĻ«ĹMŅóĶńŹä∂»ļÕ∑Ä∂®–‘ŖM––∑÷őŲľį≥ű≤Ĺ‘uĻņ÷≤»ŽőÔĎ™”√ĶńŅ…–––‘£¨Õ¨ērúp…ŔŃň”čň„ĶńŹÕŽs–‘°£‘ŕ–¬–Õ…ķőÔŠt”√šÜĶń—ņŅ∆∑N÷≤ůw—–ĺŅ÷–Õ¨ė”Ď™ģĒŖM––ń£ĒM’śĆćŅŕ«Ľ≠hĺ≥Ķń…ķőÔѶĆW–‘ń‹—–ĺŅ£¨“‘ƶ∆šĎ™”√ĚďѶŖM––»ę√ś‘uĻņ°£ŅľĎ]ĶĹĆćŽHĺ◊Ĺņ ≥őÔŖ^≥Ő÷–—ņżXĶńŖ\Ą”“鬅÷ų“™įŁņ®›SŌÚĶńČļňťŖ\Ą”ļÕā»ŌÚĶńń•ňťŖ\Ą”£¨◊ų”√‘ŕ—ņżX…ŌĶń›dļ…ŌŗĎ™Ķō”–īĻ÷Ī›dļ…ļÕÉA–Ī›dļ…[21]°£“Úīň£¨Īĺ—–ĺŅ≤…”√»żĺS”–Ōř‘™∑Ĺ∑®ń£ĒM2∑NšÜļŌĹū∑N÷≤ůw‘ŕīĻ÷ĪļÕÉA–ĪÉ…∑N›dļ…ólľĢŌ¬ĶńϙѶ∑÷≤ľ£¨≤ĘŇcāųĹy›^łŖŹó–‘ń£ŃŅĶńTi6Al4V°ĘłŁĶÕŹó–‘ń£ŃŅĶń“Ľ∑NšÜļŌĹū[22]ŖM––ƶĪ»∑÷őŲ£¨—–ĺŅ∑N÷≤ůwŹó–‘ń£ŃŅ◊ÉĽĮƶѶĆW–‘ń‹Ķń”įŪĎ£¨Źń∂ÝěťŖ@ÓźļŌĹūĶńĎ™”√—a≥šŌŗÍPĒĶďĢ°£
2°ĘĆćÚě
Ľý”ŕĪĺ’nÓ}ĹMĶń—–ĺŅ£¨÷∆āšŃňZr-30£®wt%£©TiļŌĹū°£ļŌĹūĶń÷∆āšĻ§ňáŖ^≥Ő»ÁŌ¬£ļ≤…”√’śŅ’∑«◊‘ļńŽäĽ°†t»ŘüíĶ√ĶĹľs60gĶńŤTŚV°£ěťĪ£◊CļŌĹū≥…∑÷ĶńĺýĄÚ–‘£¨ĆĘŚV◊”∑īŹÕ÷ō»Ř6īő°£ļŌĹūŚVĹõüŠČļ£®650°ś£©°ĘüŠ‹ą£®650°ś£©°Ę’śŅ’ī„Ľū£®650°ś£¨Ī£úō15min£©ę@Ķ√1.2mmļŮĶńįŚ†Óė”∆∑°£
ī„ĽūĎBė”∆∑ÖĘ’’°∂GB/T228.1-2021ĹūĆŔ≤ńŃŌņ≠…ž‘áÚěĶŕ1≤Ņ∑÷£ļ “úō‘áÚě∑Ĺ∑®°∑ŖM––ņ≠…ž‘áÚě°£ ◊Ō»£¨ Ļ”√ĺÄ«–łÓĶ√ĶĹ3ĹMņ≠…ž∆Ĺ––ė”£¨ĆĘ«–łÓĶ√ĶĹĶńī„ĽūĎBė”∆∑“ņīő Ļ”√400#°Ę800#°Ę1200#°Ę1500#ļÕ2000#Ķń…įľąŖM––īÚń•“‘ľįĺ∆ĺę≥¨¬ē«ŚŌī°£ļśł…ļůĶńė”∆∑‘ŕ “úōŌ¬ŖM––ņ≠…ž£¨ņ≠…žňŔ¬ ěť6mm/min£¨ņ≠…žŖ^≥Ő÷– Ļ”√“ż…ž”č£¨ĹYĻŻ◊ųěť∑N÷≤ůw≤ńŃŌĆŔ–‘ÖĘĒĶ°£
ÖĘ’’ Ņ◊Ņ¬Ł£®Straumann£©∑N÷≤ŌĶĹy£¨ Ļ”√Solidworks‹õľĢĹ®ŃĘ∑N÷≤ůwŌĶĹyń£–Õ£¨įŁņ®ĽýŇ_°Ę∑N÷≤ůw°ĘĻ«ĹMŅó£®∑N÷≤ůwļÜ∑QěťIM£©°£ĪMĻ‹ńŅ«į÷ųŃųĶń∑N÷≤—ņĹYėč «É…∂ő Ĺ[22‒23]£¨ěťŃňúp…ŔĚď‘ŕ ß–ßĶń∂ŗė”–‘£¨Īĺ—–ĺŅ∑N÷≤ůwĶńé◊ļőń£–Õ≤…”√“Ľ∂ő Ĺ«“ÉHŅľĎ]≤ńŃŌŐō–‘Ķń”įŪĎ°£ŠėƶŌ¬ÓMń•—ņĶńĻ«É»∑N÷≤÷őĮü£¨Ŗx»°ėňú ITI£®InstituteStraumann£¨Waldenburg£¨Switzerland£©∑N÷≤ůwěťÖĘ’’£¨∑N÷≤ůwĶńé◊ļőÖĘĒĶ»ÁąD1ňý ĺ°£∑N÷≤ůwŌŗÍPÖĘĒĶ»ÁĪŪ1ňý ĺ°£
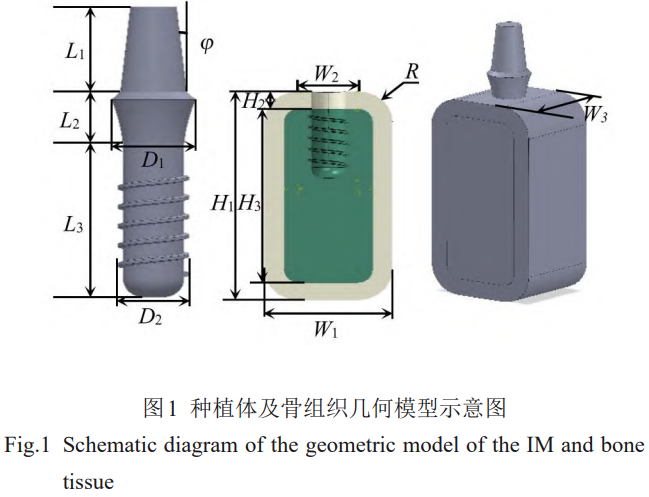
Ļ«ĹMŅó”…∆§Ŕ|Ļ«ļÕň…Ŕ|Ļ«ĹM≥…£¨É»≤Ņ «ň…Ŕ|Ļ«£¨Õ‚≤Ņł≤…w“ĽĆ”ļŮ∂»H2=2mmĶń∆§Ŕ|Ļ«£®∆§Ŕ|Ļ«ļÜ∑QěťCO£¨ň…Ŕ|Ļ«ļÜ∑QěťCA£©°£Ļ«ĹMŅóĶńĹ®ń£∑¬’’Ō¬ÓMĻ«Ĺō√ś£¨≤ĘĆĘ∆šĹŁň∆ěť∑Ĺ–ő£¨ĶęĺŖůwĶńé◊ļő≥ŖīÁĄtÖĘŅľŇRī≤ĶńĹy”čĒĶďĢ[24]£¨»ÁĪŪ1ļÕąD1ňý ĺ°£
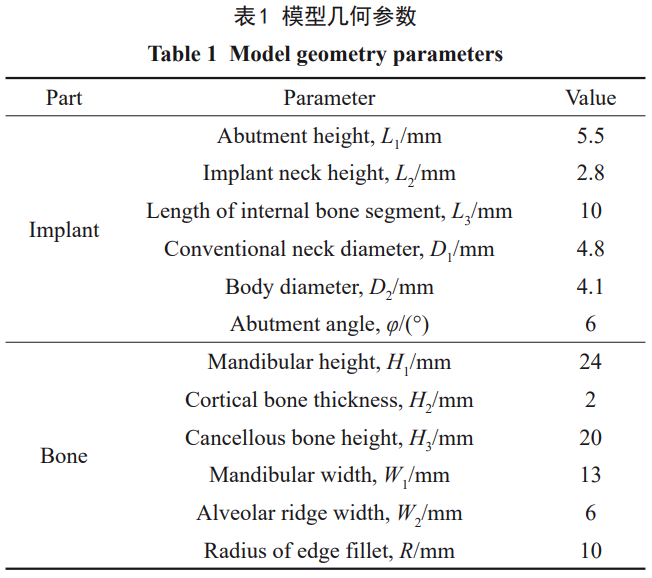
ƶ”ŕĻ«É»∑N÷≤ůw≤ńŃŌ£¨ŅľĎ]ĶĹŐé”ŕ›^–°ĶńĎ™◊ɆÓĎB£¨Ņ…ĹŁň∆ěťłųŌÚÕ¨–‘°ĘĺýĄÚĺÄŹó–‘ń£–Õ[25]°£Īĺ—–ĺŅ”čň„ňý Ļ”√Ķń≤ńŃŌ÷–“‘Ti6Al4VļÕZr24Nb◊ųěťĆ¶’’≤ńŃŌ£¨≤ńŃŌÖĘĒĶ»°◊‘őńęI[19,22]£¨“‘◊ŲłŁ»ę√śĶń∑÷őŲ°£Zr22Nb≤ńŃŌÖĘĒĶĀŪ◊‘Īĺ’nÓ}ĹMĻ§◊ų£¨łų∑N÷≤ůw≤ńŃŌĶńĆŔ–‘»ÁĪŪ2ňý ĺ°£ěť∑ĹĪ„ĪŪŖ_£¨ļůőńĺý“‘1#°Ę2#°Ę3#ļÕ4#ĀŪīķĪŪTi6Al4V°ĘZr30Ti°ĘZr22NbļÕZr24Nbłų∑N÷≤ůwń£–Õ°£
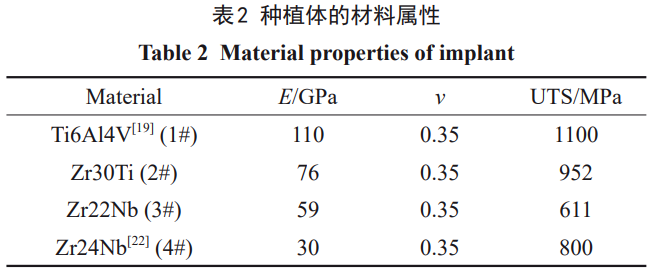
Ō¬ÓMĻ«Ķń≤ńŃŌĆŔ–‘Ô@÷Ý”įŪĎ∆šĆ¶Õ‚≤Ņ›dļ…ĶńѶĆWŪĎĎ™°£”…”ŕŹĹŌÚļÕ«–ŌÚĶńŹó–‘ń£ŃŅŌŗĹŁ≤Ę«“√ųÔ@–°”ŕŅvŌÚ£¨Ļ Ņ…’JěťĻ«ĹMŅó≤ńŃŌĆŔ–‘ěť’żĹĽłųŌÚģź–‘[25]°£Ć¶”ŕ’żĹĽłųŌÚģź–‘≤ńŃŌ£¨ń¨’J≤ńŃŌ÷Ń…Ŕ”–2āÄ’żĹĽĶńƶ∑Q∆Ĺ√ś£¨≤Ę«“≤ńŃŌĆŔ–‘™öŃĘ”ŕ√ŅāÄ∆Ĺ√śĶń∑ĹŌÚ£¨“ÚīňĻ«ĹMŅóĶń≤ńŃŌĪĺėč÷–”–9āÄŹó–‘≥£ĒĶ£¨ĺŖůw–ő Ĺěť[26–29]:
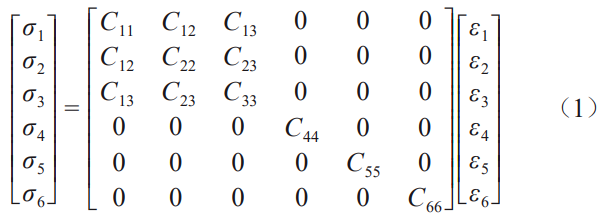
ƶ”ŕ’żĹĽłųŌÚģź–‘≤ńŃŌ£¨Źó–‘ń£ŃŅ∑÷ŃŅļÕŹó–‘≥£ĒĶ÷ģťgīś‘ŕ∂®ŃŅÍPŌĶ[30‒31]£ļ
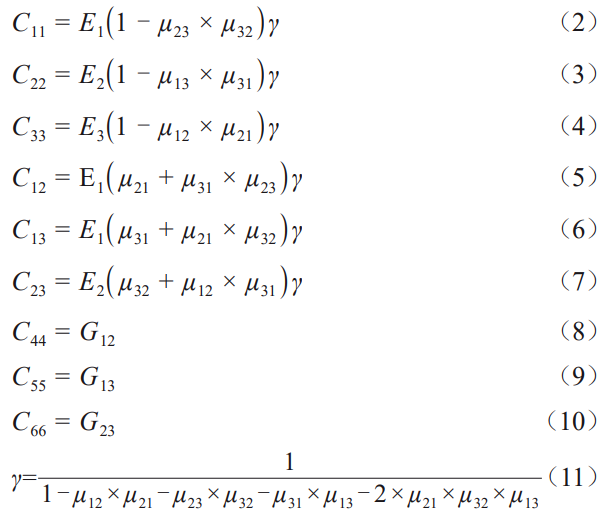
”…ĪŪ3÷–ĶńĻ«ĹMŅó≤ńŃŌÖĘĒĶ£®ĪŪ÷–Źó–‘ń£ŃŅļÕ≤īň…Ī»ĶńŌ¬ėňx°Ęy°ĘzŇc…Ō Ĺ÷–ĶńŌ¬ėň1°Ę2°Ę3ƶϙ£¨Õ¨ērŇcń£–ÕĶń◊ÝėňŌĶŌŗƶϙ£©Ņ…”čň„≥ŲĻ«ĹMŅóĶńĄā∂»ŌĶĒĶ≤Ę”√”ŕ”čň„£¨»ÁĪŪ4ňý ĺ°£
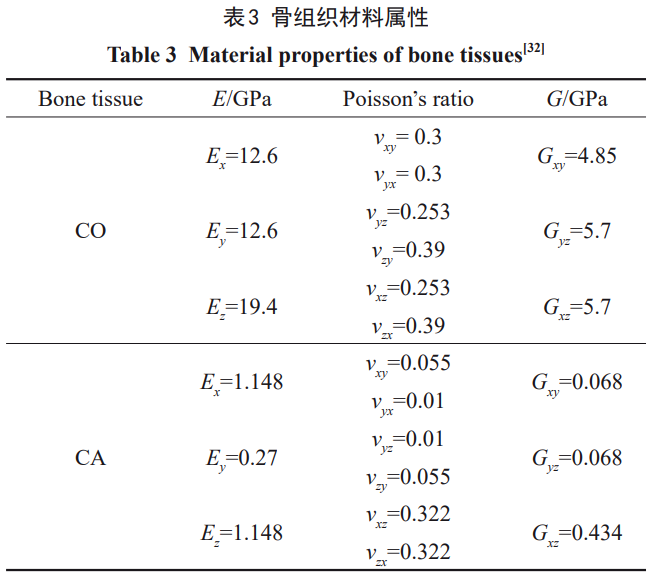
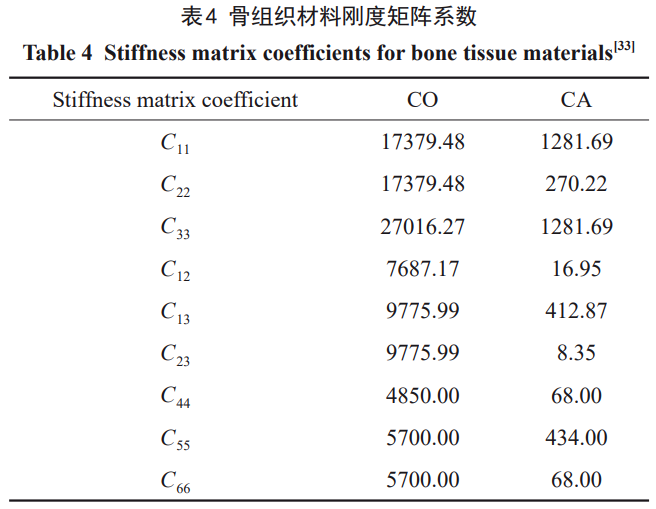
”…”ŕ∑N÷≤ůwŌĶĹy”…∂ŗāÄ≤ŅľĢĹM≥…£¨—bŇšůw÷ģťgīś‘ŕ∂ŗāÄŌŗĽ•ŇšļŌĶńĹ””|ĹÁ√ś°£Ć¶”ŕĪĺ—–ĺŅ£¨Ĺ””|ĹÁ√ś÷ų“™ěť∑N÷≤ůw-Ļ«ĹÁ√ś°Ę∆§Ŕ|Ļ«-ň…Ŕ|Ļ«ĹÁ√ś°£ěťŃňń£ĒM∑N÷≤ůw÷≤»ŽļůĶńťL∆ŕ–‘ń‹£¨ľŔ∂®∑N÷≤ůwļÕĻ«ĹMŅó÷ģťgĆć¨FÕÍ»ęĶńĻ«ĹYļŌ£¨Īĺ—–ĺŅĆĘ∆§Ŕ|Ļ«ļÕň…Ŕ|Ļ«ń£–ÕťgĶńĹ””|Óź–Õ‘O÷√ěťĹČ∂®ľs Ý£®Tie£©£¨ľīľŔ∂®Ļ«ĹMŅóťg≤Ľįl…ķŌŗƶőĽ“∆°£Ŗx»°īů–°ěť250NĶń›dļ…£¨ ©ľ””ŕľŔ‘Oěť“ßļŌĹ””|√śĶń∑N÷≤ůwĽýŇ_ĹMļŌń£–ÕŪĒ≤Ņ[34‒35]°£ľ”›d∑ĹŌÚ”–2∑N£ļ
—ō∑N÷≤ůw›SŌÚ£Ľ—ōÓa…ŗŌÚ£®ń£–Õ÷–Ķńx›S∑ĹŌÚ£©£¨ÉA–ĪĹ«∂»ÖĘŅľISO14801—ņŅ∆÷≤»ŽőÔ∆£Ąŕúy‘áėňú £¨Ŗx»°ěť30°°£ľ”›d∑ĹŌÚŇcĺWłŮ ĺ“‚ąD“äąD2°£
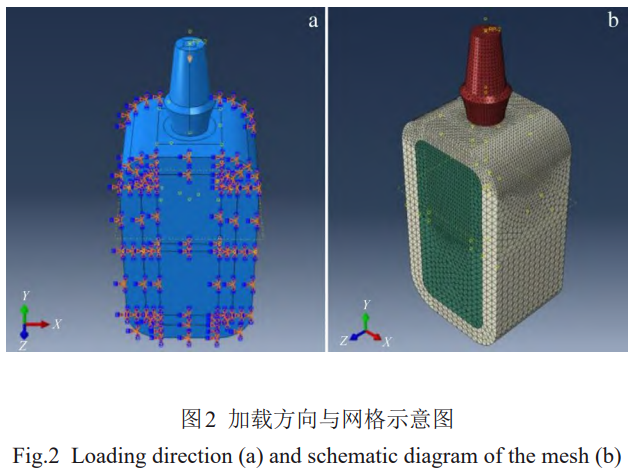
Ľý”ŕ∂Ģīőňń√śůwÜő‘™Ć¶ń£–ÕŖM––ĺWłŮĄĚ∑÷£¨Õ®Ŗ^ĺWłŮÉěĽĮī_∂®Ļ«ĹMŅóĺWłŮ≥ŖīÁľsěť1mm£¨∑N÷≤ůwĺWłŮ≥ŖīÁľs0.3mm°£Ć¶Ĺ””|ĹÁ√śĺWłŮŖM––ÉěĽĮ£¨ī_∂®Ĺ””|ĹÁ√śŐé∑N÷≤ůw≤Ņ∑÷ĺWłŮ≥ŖīÁěť0.2mm£¨Ļ«ĹMŅó≤Ņ∑÷ĺWłŮ≥ŖīÁěť0.15mm°£ń£–ÕĺWłŮÜő‘™ĒĶ»ÁĪŪ5ňý ĺ°£
3°ĘĆćÚěĹYĻŻ
3.1°°∑N÷≤ůwľįĻ«ĹMŅóĶńϙѶ∑÷≤ľ
īĻ÷Ī›dļ…Ō¬łųĹMń£–Õ÷–∑N÷≤ůwĶńMisesϙѶ∑÷≤ľ»ÁąD3ňý ĺ£¨Ď™Ń¶∑÷≤ľŕÖĄ›Ōŗň∆£¨Ď™Ń¶ľĮ÷–Ňc◊ÓīůϙѶőĽ÷√ĺýěť∑N÷≤ůwÓi≤ŅÖ^”Ú°£Õ¨ė”£¨łųĹMń£–Õ÷–∆§Ŕ|Ļ«ļÕň…Ŕ|Ļ«ĺŖ”–Ōŗň∆ĶńϙѶ∑÷≤ľ°£∆§Ŕ|Ļ«Ňcň…Ŕ|Ļ«…ŌĪŪ√śŖÖĺČĺýīś‘ŕϙѶľĮ÷–£¨ň…Ŕ|Ļ«ĶńĶŕ“Ľ¬›ľyŐéŌŗ›^∆šňŻőĽ÷√“≤ĪŪ¨F≥Ų›^łŖĶńϙѶ°£ŌŗĪ»∆šňŻ≤ńŃŌ£¨ÉHŹó–‘ń£ŃŅěť30GPaĶń4#ń£–Õ£®Zr24Nb£©‘ŕĻ«ĹMŅó≥Ų¨F“Ľ∂®ĶńϙѶ∑÷≤ľÖ^ĒUīů°£
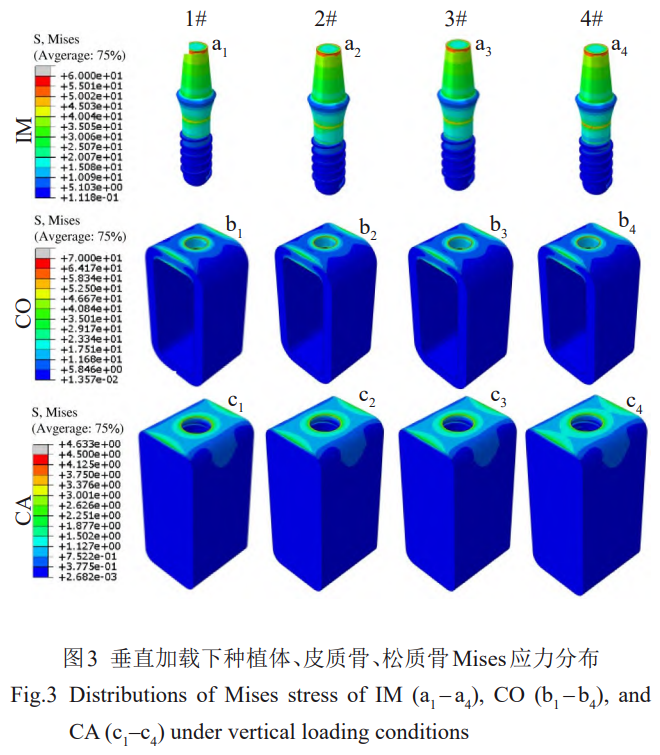
łųń£–ÕĹYĻŻĶń≤Óģź÷ų“™ĪŪ¨F‘ŕ◊ÓīůϙѶ÷Ķ°£»ÁĪŪ6ňý ĺ£¨īĻ÷Īľ”›dólľĢŌ¬£¨1#£®110GPa£©°Ę2#£®76GPa£©°Ę3#£®59GPa£©°Ę4#£®30GPa£©∑N÷≤ůwĶń◊ÓīůϙѶ∑÷Ąeěť75°Ę77°Ę79°Ę85MPa£¨‘ŕ∆§Ŕ|Ļ«÷–ģa…ķĶń◊ÓīůMisesϙѶ∑÷Ąeěť86°Ę89°Ę91°Ę98MPa£¨‘ŕň…Ŕ|Ļ«÷–ģa…ķĶń◊ÓīůMisesϙѶ≤ÓĄe≤Ľīů£¨∑÷Ąeěť4.63°Ę4.57°Ę4.51°Ę4.23MPa£¨∑N÷≤ůwāųŖfĶńϙѶ÷ų“™”…∆§Ŕ|Ļ«≥– ‹°£∑N÷≤ůwļÕ∆§Ŕ|Ļ«ĶńϙѶľĮ÷–≥Ő∂»ļÕ◊ÓīůϙѶ÷ĶĺýŽS÷ÝŹó–‘ń£ŃŅĶńĹĶĶÕ∂Ý‘Ųľ”£¨ň…Ŕ|Ļ«Ąt≥ ¨FŌŗ∑īĶńŕÖĄ›°£
ÉA–Ī›dļ…Ō¬łųĹMń£–ÕĶńϙѶ∑÷≤ľŌŗň∆£®ąD4£©°£Ļ«ĹMŅóϙѶ√ųÔ@ľĮ÷–‘ŕ“Ľā»£¨∑N÷≤ůwĄt‘ŕ—ōľ”›d∑ĹŌÚĶńÉ…ā»ĺýīś‘ŕϙѶľĮ÷–°£1#∑N÷≤ůwĶńÓi≤ŅϙѶÖ^Ņ…Ŗ_ĶĹĶ໿¬›ľy£¨2#°Ę3#Ąt‘ŕĶŕ∂Ģ°Ę»ż¬›ľyťg£¨4#ÉH‘ŕĶŕ“Ľ¬›ľy°£Õ¨ēr£¨1#°Ę2#°Ę3#°Ę4#∑N÷≤ůw‘ŕÉA–Ī›dļ…Ō¬Ķń◊ÓīůϙѶ∑÷Ąeěť336°Ę346°Ę355°Ę385MPa°£ŽS÷Ý÷≤»Ž≤ńŃŌĶńŹó–‘ń£ŃŅĹĶĶÕ£¨∑N÷≤ůwÓi≤ŅĶńϙѶľĮ÷–≥Ő∂»‘Ųľ”°£
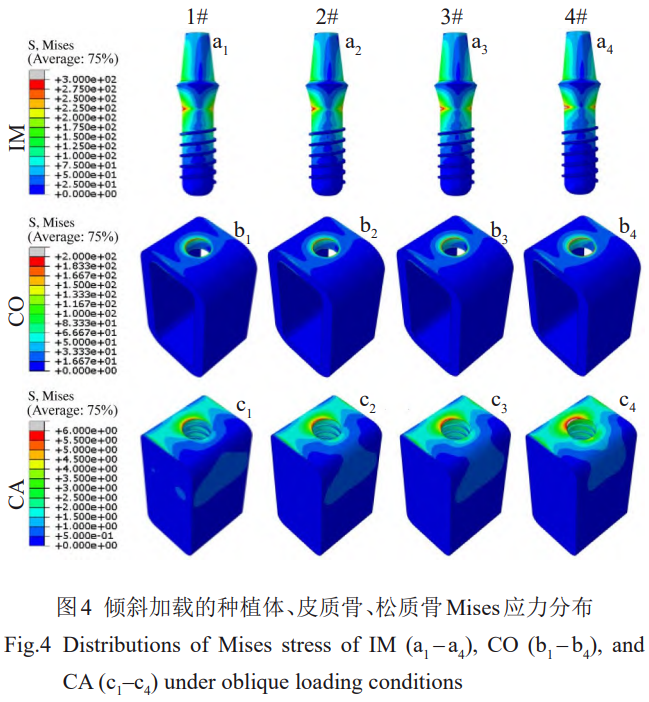
ƶ”ŕ∑N÷≤ůw‘ŕ∆§Ŕ|Ļ«É»ĪŪ√śģa…ķĶńīů”ŕ50MPaĶńϙѶÖ^∑∂áķ£¨1#ģa…ķĶńŌŗϙϙѶÖ^īů–°ľsěť∆§Ŕ|Ļ«ļŮ∂»Ķń1/2£¨2#ģa…ķĶńŌŗϙϙѶÖ^īů–°ľsĶ»”ŕ∆§Ŕ|Ļ«ļŮ∂»£¨3#ļÕ4#ģa…ķĶńŌŗϙϙѶÖ^ŖM“Ľ≤ĹôMŌÚĒUīů°£Ć¶”ŕň…Ŕ|Ļ«ĪŪ√śīů”ŕ2MPaĶńϙѶÖ^£¨ŌŗĪ»”ŕ1#£¨2#°Ę3#°Ę4#∑N÷≤ůwģa…ķĶńϙѶÖ^√ųÔ@ĒUīů°£Ć¶”ŕň…Ŕ|Ļ«÷≤»ŽőĽ÷√¬›ľyťgÉ»ĪŪ√ś£¨2#°Ę3#°Ę4#ĶńϙѶ£®2~3MPa£©Ķń∑∂áķ÷ūĚuĒUīů°£»ÁĪŪ6ňý ĺ£¨ŇcīĻ÷Ī›dļ…Ķń“鬅ŌŗÕ¨£¨∑N÷≤ůwļÕ∆§Ŕ|Ļ«Ķń◊ÓīůϙѶ÷ĶŽS÷ÝŹó–‘ń£ŃŅĶńĹĶĶÕ∂Ý‘Ųľ”°£»Ľ∂Ý£¨1#°Ę2#°Ę3#°Ę4#∑N÷≤ůw‘ŕň…Ŕ|Ļ«ģa…ķĶń◊ÓīůϙѶ÷Ķ∑÷Ąeěť6.57°Ę6.56°Ę6.57°Ę6.79MPa£¨Ąt «Ō»úp–°ļů‘Ųľ”£¨∑N÷≤ůwŹó–‘ń£ŃŅěť76GPaēr◊Ó–°°£‘ŕ2∑N›dļ…ólľĢŌ¬£¨Ļ«ĹMŅó÷–ĶńϙѶ÷ų“™”…∆§Ŕ|Ļ«≥–ďķ°£ÉA–Īľ”›d‘ŕ∑N÷≤ůwļÕ∆§Ŕ|Ļ«ňýģa…ķĶń◊ÓīůϙѶ“™√ųÔ@łŖ”ŕīĻ÷Īľ”›d£¨łų∑N÷≤ůwĶń◊ÓīůϙѶľsěťīĻ÷Ī›dļ…Ō¬Ķń4.5Ī∂£¨1#°Ę2#°Ę3#ľį4#ń£–Õ÷–∆§Ŕ|Ļ«Ķń◊ÓīůϙѶľsěťīĻ÷Ī›dļ…Ō¬Ķń2.6Ī∂°Ę2.9Ī∂°Ę3.2Ī∂°Ę4.1Ī∂£¨Ď™Ń¶‘Ųľ”∑ý∂»÷ūĚu‘Ųīů°£
≤Ľ’ď «īĻ÷Īľ”›dŖÄ «ÉA–Īľ”›d£¨Óa…ŗŌÚ£®ń£–Õ÷–Ķńx›S∑ĹŌÚ£©ĶńϙѶ‘ŕ¬∑ŹĹA-BĶń«į3āÄĻĚŁcÉ»—łňŔĹĶĶÕ£¨Ŗ@ «”…”ŕ‘ŕĹ””|√ś Ļ”√Ńň≤Ľįl…ķŌŗƶőĽ“∆ĶńĹČ∂®ľs ÝŹń∂ÝĆß÷¬Ķŕ1āÄÜő‘™É»ĶńϙѶ՛∂»›^īů£¨Ķ√ĶĹĶńĹYĻŻ›^ěťĪ£ ō°£»Ľ∂Ý£¨Ď™Ń¶‘ŕĹõöv›^ěť—łňŔĶńĹĶĶÕļů÷ūĚuŕÖ”ŕ∆Ĺ台£
īĻ÷Ī›dļ…Ō¬£¨∆§Ŕ|Ļ«‘ŕÓa…ŗŌÚ¬∑ŹĹA-BĶńĶŕ3āÄĻĚŁcļůĶńϙѶ∑∂áķěť5~25MPa£ĽÉA–Ī›dļ…Ō¬£¨∆§Ŕ|Ļ«‘ŕÓa…ŗŌÚ¬∑ŹĹA-EĶńĶŕ3āÄĻĚŁcļůĶńϙѶ∑∂áķěť0~80MPa£Ľ≤Ę«“∑N÷≤ůwŹó–‘ń£ŃŅĶńĹĶĶÕ ĻĶ√∆§Ŕ|Ļ«Ď™Ń¶”–ňý‘Ųľ”£®ąD5b°Ę5e£©°£ŌŗĪ»”ŕÓa…ŗŌÚ£¨ĹŁŖh÷–∑ĹŌÚ£®ń£–Õ÷–Ķńz›S∑ĹŌÚ£©ĶńϙѶ◊ÉĽĮ’Żůw›^ěťļÕĺŹ£¨īĻ÷Īľ”›d£®¬∑ŹĹC-D£©ļÕÉA–Īľ”›d£®¬∑ŹĹC-F£©ĶńϙѶĺý–°”ŕ100MPa£¨ÉA–Īľ”›dģa…ķĶń◊ÓīůϙѶ£®őĽ÷√C£©ÉHĪ»īĻ÷Īľ”›dłŖľs13%£®ąD5c°Ę5f£©°£
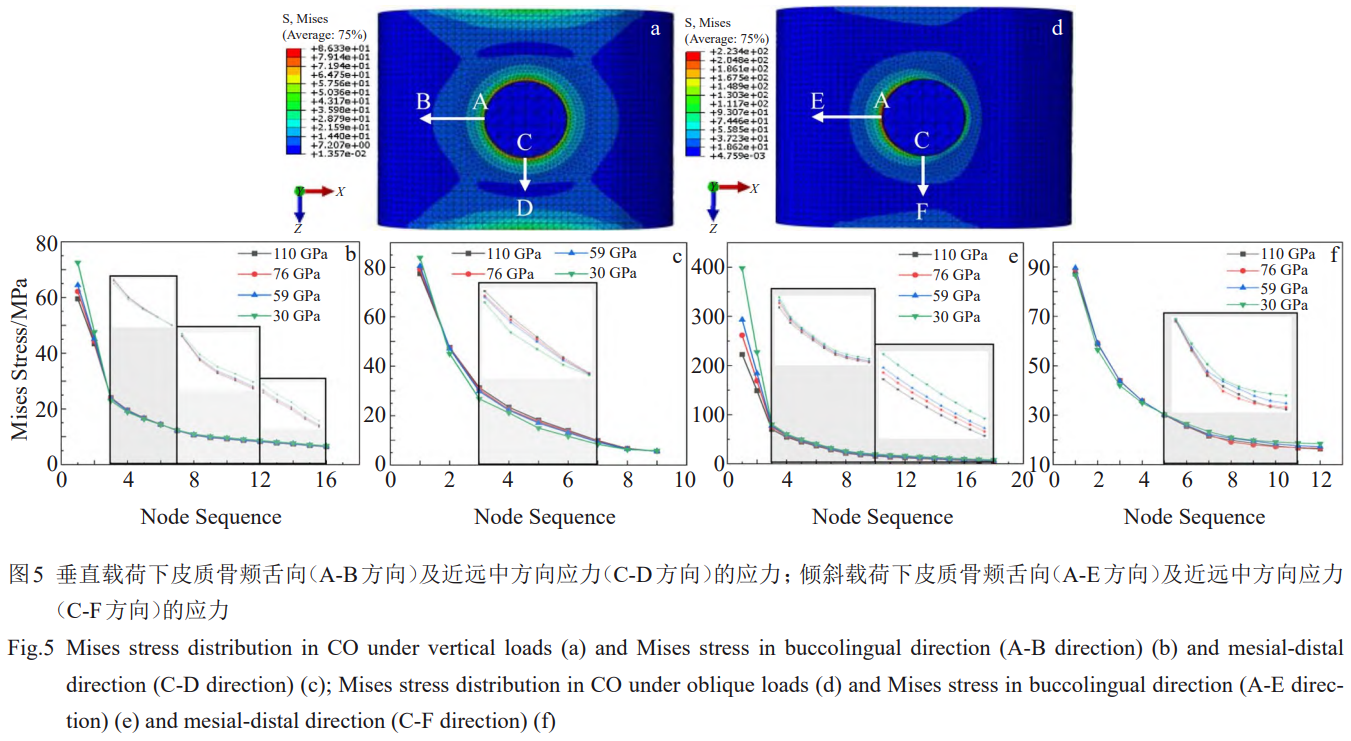
»Ľ∂Ý£¨ÉA–Īľ”›d‘ŕÓa…ŗŌÚģa…ķĶń◊ÓīůϙѶ£®őĽ÷√A£©Ī»īĻ÷Īľ”›dłŖ2.7~4.5Ī∂°£“Ľ∑Ĺ√ś£¨2∑Nľ”›dólľĢŌ¬ĶńϙѶľĮ÷–őĽ÷√≤ĽÕ¨£¨īĻ÷Īľ”›dērϙѶľĮ÷–ŐéőĽ”ŕĹŁŖh÷–∑ĹŌÚ£®őĽ÷√C£©£¨∂ÝÉA–Īľ”›dērĄtőĽ”ŕÓa…ŗŌÚ£®őĽ÷√A£©£ĽŃŪ“Ľ∑Ĺ√ś£¨īĻ÷Īľ”›dērϙѶ‘ŕ∆§Ŕ|Ļ«÷≤»Ž≤ŅőĽŖÖĺČĶń∑÷≤ľŌŗĪ»”ŕÉA–Īľ”›dłŁěťĺýĄÚ£¨ÉA–Īľ”›dērϙѶľĮ÷–‘ŕ∆§Ŕ|Ļ«Ķń“Ľā»£¨“ÚīňŖ@∑N›dļ…Ļ§õrƶ”ŕ∆§Ŕ|Ļ« «“Ľ∑NłŁěťźļŃ”Ķń«ťõr£¨Ķę∑N÷≤ůwĎ™“ņ»ĽĪ£≥÷Ńľļ√Ķń–‘ń‹£¨“‘ŖmĎ™ĆćŽHŅŕ«ĽĎ™”√÷–Ņ…ń‹≥Ų¨FĶń≤ĽŃľ›dļ…ólľĢ°£»Ľ∂Ý£¨Ć¶”ŕ∆§Ŕ|Ļ«ĪŪ√śĶńϙѶ◊ÉĽĮ£¨łųń£–ÕťgĶń≤Óģź›^–°£¨√ųÔ@Ķń≤Óģź÷ų“™‘ŕ”ŕ∆§Ŕ|Ļ«Ňc∑N÷≤ůwĹ””|ĹÁ√ś“‘ľį∆§Ŕ|Ļ«◊ÓīůϙѶ£¨ģa…ķ≤ÓģźĶń‘≠“ÚŅ…ń‹ «”…”ŕ∆§Ŕ|Ļ«ĪŪ√śěť◊‘”…ĪŪ√ś£¨∂Ý∆§Ŕ|Ļ«Ňc∑N÷≤ůwťgīś‘ŕÕÍ»ęľs ÝĶńĹ””|°£
3.2°°∑N÷≤ůwľįĻ«ĹMŅóĶń◊ÓīůϙѶ∑÷őŲ
‘ŕÉA–Ī›dļ…Ō¬£¨∑N÷≤ůwĶń◊ÓīůϙѶ›^łŖ£¨≤ĘŽS÷Ýń£ŃŅĶńĹĶĶÕϙѶŌŗĎ™‘Ųľ”£¨Ķęĺý–°”ŕłų≤ńŃŌĶńŅĻņ≠Źä∂»£¨«“◊ÓīůϙѶ’ľ∆šŹä∂»ĶńįŔ∑÷Ī»ĺý–°”ŕ60%£®ąD6£©°£2∑N›dļ…ólľĢŌ¬£¨◊ÓīůMisesϙѶĺýŽS÷ÝŹó–‘ń£ŃŅĶńĹĶĶÕ∂Ý‘Ųľ”£¨≤Ę«“ÉA–Ī›dļ…Ō¬Ķń◊ÉĽĮłŁěť√ųÔ@£®ąD7a°Ę7d£©°£ŅľĎ]ĶĹĻ«ĹMŅóŅ…ĹŁň∆ěťīŗ–‘≤ńŃŌ[31]£¨ģĒ◊Óīů÷ųϙѶŖ_ĶĹĽÚ≥¨Ŗ^≤ńŃŌĶńŅĻņ≠Źä∂»ĽÚŅĻČļŹä∂»ēr£¨īŗ–‘≤ńŃŌÕýÕýēĢįl…ķÕĽ»Ľ∆∆Čń£¨“Úīňƶ∆§Ŕ|Ļ«Ķń◊Óīů÷ųϙѶŖM––∑÷őŲ°£2∑N›dļ…ólľĢŌ¬£¨∆§Ŕ|Ļ«÷–Ķń◊ÓīůČļϙѶ÷Ķĺýīů”ŕ◊Óīůņ≠ϙѶ÷Ķ°£
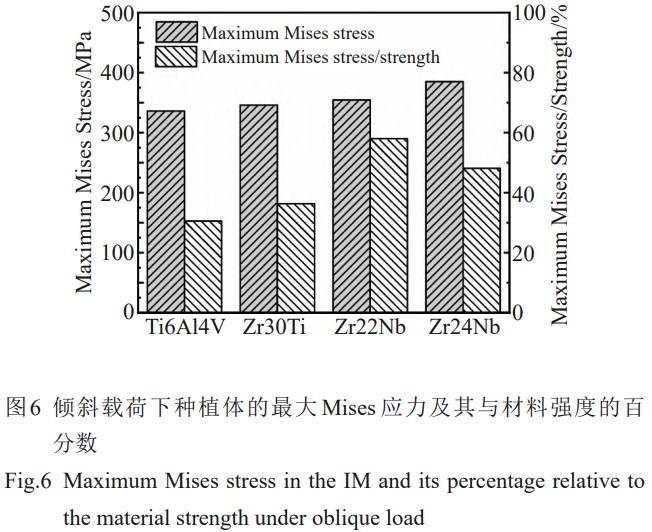
īĻ÷Ī›dļ…Ō¬£¨◊Óīůņ≠ČļϙѶ∑∂áķěť–150~100MPa£ĽÉA–Ī›dļ…Ō¬£¨◊Óīůņ≠ČļϙѶ∑∂áķěť–700~500MPa£®ąD7b°Ę7e£©°£”…«į ŲƶMisesϙѶĶń∑÷őŲĪŪ√ų£¨‘ŕ∆§Ŕ|Ļ«÷≤»Ž≤ŅőĽĶńŖÖĺČīś‘ŕ›^īůĶńϙѶľĮ÷–£¨Ŗ@ «”…”ŕé◊ļőń£–Õ‘ŕīňŐéěť÷ĪĹ«£¨īś‘ŕ∆śģźŁc£®ľī”čň„ϙѶ÷ĶŕÖ”ŕüołFīů£©°£ěťŃňŅň∑Ģ”čň„ÜĖÓ}≤ĘĶ√ĶĹłŁĺŖīķĪŪ–‘ļÕ’śĆć–‘ĶńĹYĻŻ£¨‘ŕŇŇ≥żŃň0.1%Ķń∆śģźĻĚŁcļůƶ◊Óīů÷ųϙѶŖM––ŃňĹy”č°£īĻ÷Ī›dļ…Ō¬£¨ŌŗĪ»”ŕ1#£¨2#°Ę3#°Ę4#∑N÷≤ůw‘ŕ∆§Ŕ|Ļ«Ķń◊ÓīůMisesϙѶ¬‘”–ĹĶĶÕ£¨◊ÓīůMisesϙѶ∑∂áķěť35.96~39.29MPa£¨◊Óīůņ≠ČļϙѶ∑∂áķěť–43.68~–39.20MPa£ĽÉA–Ī›dļ…Ō¬£¨2#°Ę3#°Ę4#∑N÷≤ůw‘ŕ∆§Ŕ|Ļ«ģa…ķĶń◊ÓīůMisesϙѶŌŗĪ»”ŕ1#‘Ųľ”£¨◊ÓīůMisesϙѶ∑∂áķěť99~123MPa£¨◊Óīůņ≠ČļϙѶ∑∂áķěť–188~130MPa£®ąD7b°Ę7e£©°£īĻ÷Ī›dļ…ļÕÉA–Ī›dļ…Ō¬∆§Ŕ|Ļ«Ķń◊ÓīůMisesϙѶĺýŽSŹó–‘ń£ŃŅĶńĹĶĶÕ∂Ý‘Ųľ”≤Ę≥ ¨F›pőĘĶń∑«ĺÄ–‘ŐōŁc°£
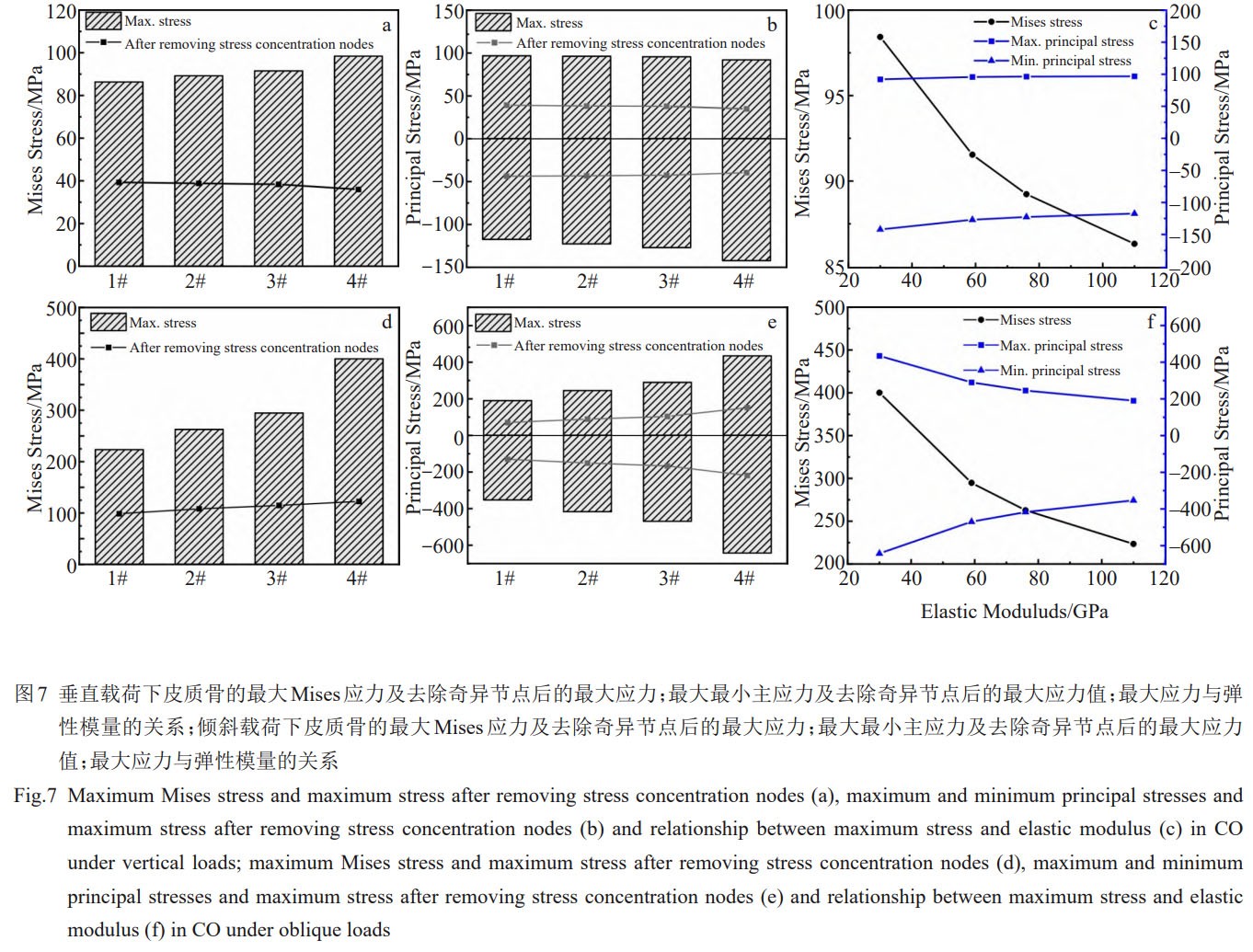
ƶ”ŕ∆§Ŕ|Ļ«÷–Ķń÷ųϙѶ£¨◊ÓīůČļϙѶ÷ĶŽS÷Ý÷≤»Ž≤ńŃŌŹó–‘ń£ŃŅĶńĹĶĶÕ∂Ý‘Ųľ”£¨◊Óīůņ≠ϙѶ÷Ķ‘ŕīĻ÷Īľ”›dērŽS÷ÝŹó–‘ń£ŃŅ‘Ųľ”∂Ýúp–°£¨ÉA–Īľ”›dērĄtŽSŹó–‘ń£ŃŅĶń‘Ųľ”∂Ý‘Ųľ”£®ąD7c°Ę7f£©°£Ŗ@ «”…”ŕ2∑N›dļ…ólľĢŌ¬∆§Ŕ|Ļ«Ķń◊Óīůņ≠ϙѶőĽ÷√≤ĽÕ¨£¨»ÁąD8c1~8c4ļÕąD9c1~9c4ňý ĺ°£
3.3°°∑N÷≤ůwŹó–‘ń£ŃŅƶ∑N÷≤ůw-Ļ«ĹÁ√śĎ™Ń¶Ķń”įŪĎ
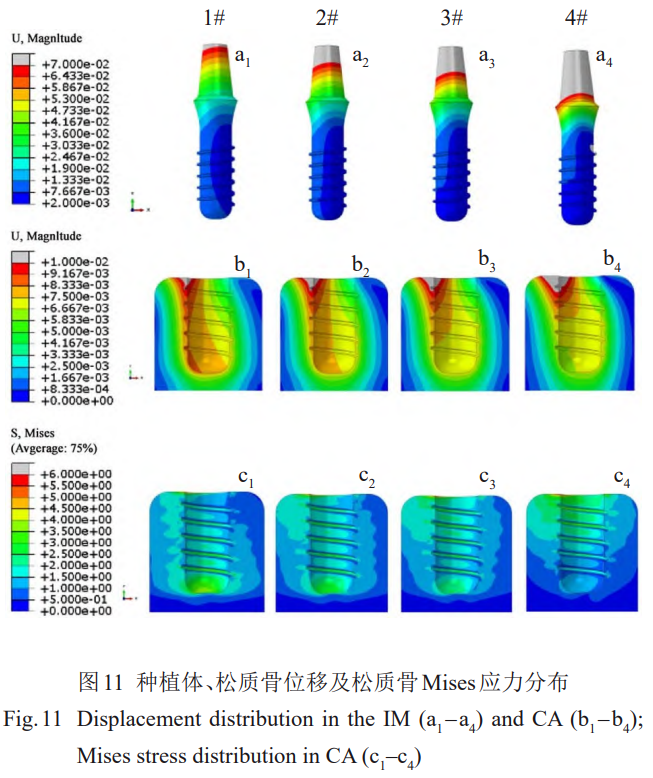
īĻ÷Īľ”›dēr£¨∑N÷≤ůw-∆§Ŕ|Ļ«ĹÁ√śŐéĶńϙѶľĮ÷–őĽ”ŕ∆§Ŕ|Ļ«…ŌŌ¬É…∂ň£¨Õ¨ēr «∆§Ŕ|Ļ«įl…ķé◊ļőÕĽ◊ÉĶńőĽ÷√°£∆§Ŕ|Ļ«…Ō∂ňϙѶľĮ÷–ŐéĶńMisesϙѶ «∆§Ŕ|Ļ«÷–Ķń◊Óīů÷Ķ£¨ŽS÷ÝŹó–‘ń£ŃŅĶńúp–°∂Ý‘Ųľ”°£1#°Ę2#°Ę3#°Ę4#∑N÷≤ůw‘ŕ∆§Ŕ|Ļ«Ō¬∂ňĶń◊ÓīůMisesϙѶ÷Ķ∑÷Ąeěť71°Ę68°Ę62°Ę60MPa£¨ŽS÷Ý∑N÷≤ůwŹó–‘ń£ŃŅĶńĹĶĶÕ∂Ý÷ūĚuúp–°°£
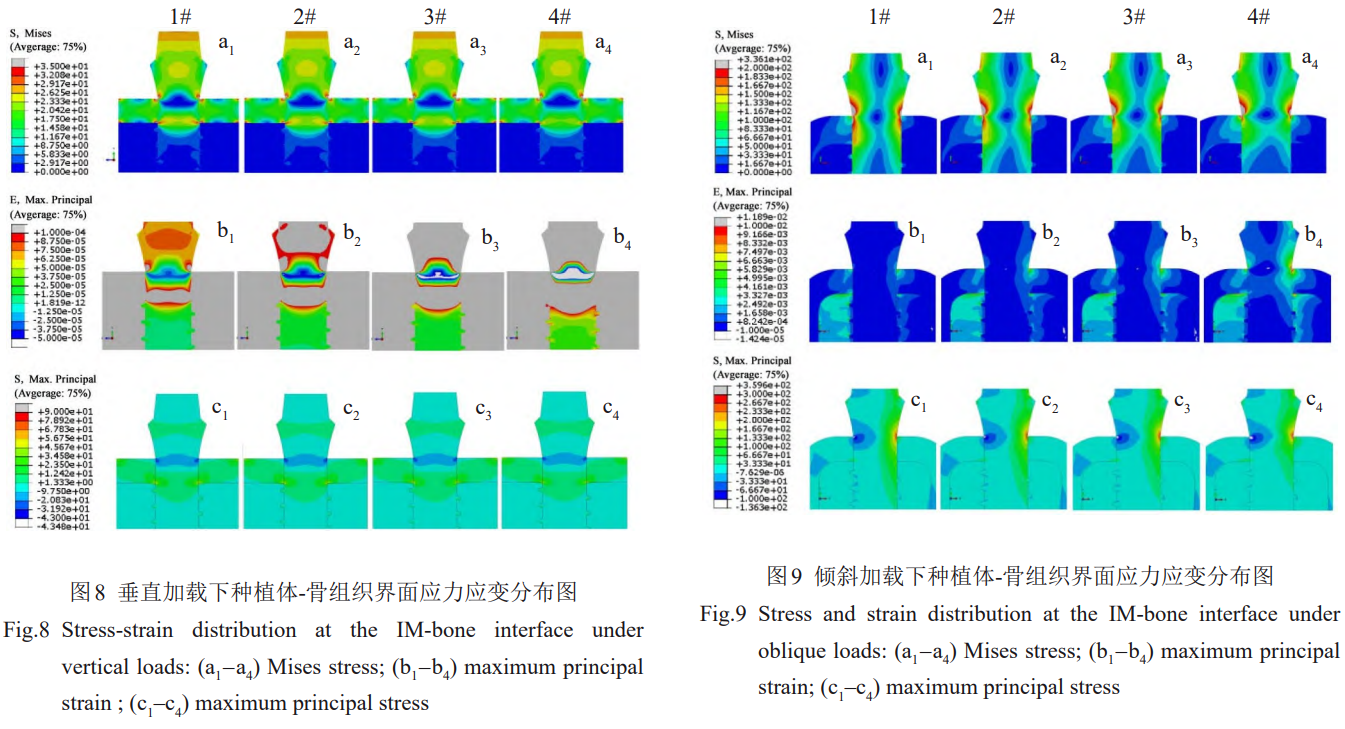
ƶ”ŕŇc∆§Ŕ|Ļ«Ō¬∂ňĹ””|Ķń∑N÷≤ůwÉ»≤Ņ£¨īů”ŕ23MPaĶńϙѶÖ^ôMī©∑N÷≤ůw£¨2#°Ę3#∑N÷≤ůwÉ»‘ďϙѶÖ^∑∂áķ÷ūĚuŅs–°£¨4#∑N÷≤ůwÉ»‘ďϙѶÖ^“—≤Ľ√ųÔ@£®ąD8a1~8a4£©°£Ć¶”ŕ◊Óīů÷ųϙѶĶń∑÷≤ľ£¨łųń£–Õťgõ]”–√ųÔ@≤ÓĄe£¨Ķę◊Óīůņ≠ČļϙѶĺýŽS÷ÝŹó–‘ń£ŃŅĶńĹĶĶÕ∂Ý‘Ųľ”£®ąD8c1~8c4£©°£łų∑N÷≤ůwÉ»≤ŅĎ™◊ÉĺýěťČļĎ™◊É£¨1#°Ę2#°Ę3#°Ę4#∑N÷≤ůwÉ»≤ŅĶńĎ™◊É∑÷Ąeľsěť–2.9×10-5°Ę–4.8×10-5°Ę–6.8×10-5°Ę–1.2×10-4£¨ČļĎ™◊ÉŽS÷ÝŹó–‘ń£ŃŅĶńĹĶĶÕ∂Ý‘Ųľ”£®ąD8b1~8b4£©°£
ÉA–Īľ”›dēr£¨∆§Ŕ|Ļ«÷–ϙѶľĮ÷–Ö^”Ú÷ų“™őĽ”ŕ…Ō∂ň£¨≤Ę«“‘ďÖ^”Úīů”ŕ50MPaĶńϙѶÖ^√ųÔ@ŽS÷Ý∑N÷≤ůwŹó–‘ń£ŃŅĶńĹĶĶÕ∂ÝĒUīů°£Õ¨ēr£¨∑N÷≤ůwÉ…ā»īů”ŕ150MPaĶńłŖϙѶÖ^ŽS÷Ý∑N÷≤ůwŹó–‘ń£ŃŅĶńĹĶĶÕ√ųÔ@Ņs–°£¨Ď™Ń¶ľĮ
÷–≥Ő∂»‘Ųľ”£®ąD9a1~9a4£©°£∑N÷≤ůwÉ…ā»Ķń◊Óīůņ≠ČļĎ™Ń¶Õ¨ė”ŽS÷Ý∑N÷≤ůwŹó–‘ń£ŃŅĶńĹĶĶÕ∂Ý‘Ųľ”£¨3#°Ę4#∑N÷≤ůwÉ»≤Ņīů”ŕ100MPaĶńČļϙѶÖ^ĪŪ¨F≥ŲĒUīůŕÖĄ›£®ąD9c1~9c4£©°£2#°Ę3#°Ę4#∑N÷≤ůwĶńÉ»≤Ņ≥Ų¨F◊Óīů÷ųĎ™◊É÷Ķīů”ŕ1×10-5ĶńČļĎ™◊ÉÖ^£¨3#∑N÷≤ůwÉ»◊Óīů÷ųĎ™◊É÷Ķīů”ŕ1.7×10-3ĶńĎ™◊ÉÖ^≥Ų¨FôMŌÚĒUīůĶńŕÖĄ›£¨4#∑N÷≤ůwÉ»‘ďĎ™◊ÉÖ^“—‘ŕ∑N÷≤ůwÉ»≤ŅôMŌÚ∑÷≤ľ°£1#°Ę2#°Ę3#°Ę4#∑N÷≤ůwĶńÉ»≤Ņ◊Óīů÷ųĎ™◊É∑÷Ąeěť–1.4×10-5°Ę–2.8×10-5°Ę–3.7×10-5°Ę–6.9×10-5£¨ÉA–Ī›dļ…Ō¬2#°Ę3#ļÕ4#∑N÷≤ůwÓi≤ŅÉ»Ķń◊ÓīůĎ™◊É∑÷Ąe «1#Ķń2Ī∂°Ę2.6Ī∂°Ę4.9Ī∂°£
īĻ÷Ī›dļ…Ō¬£¨1#°Ę2#°Ę3#°Ę4#∑N÷≤ůw‘ŕ∑N÷≤ůw-∆§Ŕ|Ļ«ĹÁ√śĶń∆§Ŕ|Ļ«…ŌŌ¬É…∂ňŇŇ≥żŖÖĺČϙѶľĮ÷–Üő‘™ļůĶńϙѶ≤Óīů–°∑÷Ąeľsěť10.7°Ę10.8°Ę11°Ę11.7MPa£¨ŌŗĎ™∑N÷≤ůw…ŌŌ¬É…∂ňĶńϙѶ≤Óīů–°ľsěť13.2°Ę7.7°Ę7.8°Ę9.0MPa°£ģĒ÷≤»Ž≤ńŃŌěťTi6Al4Vēr£¨∑N÷≤ůw-∆§Ŕ|Ļ«ĹÁ√śÉ…ā»ĶńϙѶ≤Ó ģ∑÷√ųÔ@°£ģĒ÷≤»Ž≤ńŃŌĶńŹó–‘ń£ŃŅĹĶĶÕēr£¨ĹÁ√śĎ™Ń¶≤Ó√ųÔ@úp–°£¨«“2#°Ę3#°Ę4#ń£–ÕĶń’ŻůwϙѶ÷ĶŌŗ›^”ŕ1#ń£–Õúp–°Ô@÷Ý°£»Ľ∂Ý£¨Ć¶4#ń£–Õ£®E=30GPa£©£¨ĹÁ√śÉ…ā»∆§Ŕ|Ļ«ļÕ∑N÷≤ůwĶńϙѶŌŗĪ»”ŕ2#£®E=76GPa£©ļÕ3#£®E=59GPa£©ń£–Õĺý”–ňý‘Ųľ”£®ąD10b£©°£
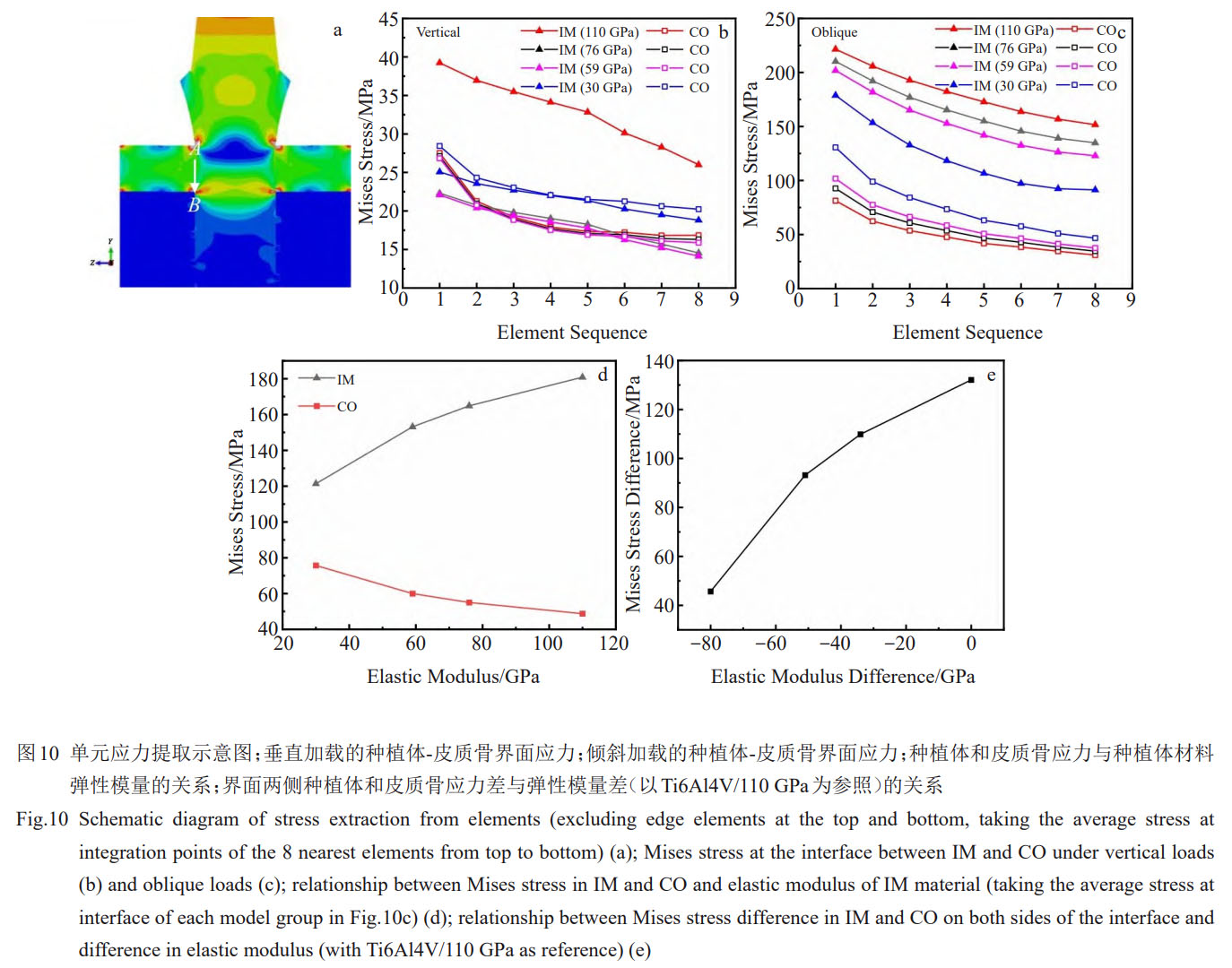
ÉA–Ī›dļ…Ō¬£¨ŽS÷Ý÷≤»Ž≤ńŃŌŹó–‘ń£ŃŅĶńĹĶĶÕ£¨ĹÁ√śĶń∑N÷≤ůw“Ľā»Ď™Ń¶úp–°£¨Ļ«ĹMŅó“Ľā»Ď™Ń¶‘Ųľ”£¨ĹÁ√śÉ…ā»ĶńϙѶ≤Ó√ųÔ@úp–°£®ąD10c£©°£1#°Ę2#°Ę3#°Ę4#∑N÷≤ůw-Ļ«ĹÁ√śŐéĶń∑N÷≤ůw∆ĹĺýMisesϙѶ÷Ķ∑÷Ąeěť181°Ę165°Ę153°Ę121MPa£¨∆§Ŕ|Ļ«Ķń∆ĹĺýMisesϙѶ∑÷Ąeěť49°Ę55°Ę60°Ę76MPa£¨∑N÷≤ůwļÕ∆§Ŕ|Ļ«ĶńϙѶ≤Ó∑÷Ąeěť132°Ę110°Ę93°Ę46MPa°£∑N÷≤ůwļÕ∆§Ŕ|Ļ«ĶńϙѶ◊ÉĽĮŽSŹó–‘ń£ŃŅĶńĹĶĶÕ◊ÉĽĮŕÖĄ›≤ĽÕ¨£¨∑N÷≤ůwϙѶĹĶĶÕ∂Ý∆§Ŕ|Ļ«Ď™Ń¶‘Ųľ”£¨ĹÁ√śÉ…ā»ĶńϙѶ≤ÓŌŗĎ™ĹĶĶÕ£¨ĹÁ√ś…ŌĶń∆ĹĺýϙѶľįĹÁ√śÉ…ā»Ď™Ń¶≤ÓŽS∑N÷≤ůwŹó–‘ń£ŃŅĶń◊ÉĽĮ∂Ý≥ √ųÔ@Ķń∑«ĺÄ–‘◊ÉĽĮ£®ąD10d°Ę10e£©°£
ÉA–Ī›dļ…◊ų”√Ō¬£¨ŽS÷Ý∑N÷≤ůw≤ńŃŌŹó–‘ń£ŃŅĶńĹĶĶÕ£¨∑N÷≤ůwĶńłŖőĽ“∆Ö^÷ūĚuŌÚÓi≤Ņ“∆Ą”£¨∑N÷≤ůwĻ«É»∂őĶńőĽ“∆∑÷≤ľĺýĄÚ–‘ĹĶĶÕ£®ąD11a1~11a4£©°£1#°Ę2#∑N÷≤—ņ÷≤»ŽĶńň…Ŕ|Ļ« ‹Čļā»É»ĪŪ√śőĽ“∆īů”ŕ7.5×10-3mm£¨ŽS÷Ý∑N÷≤ůwŹó–‘ń£ŃŅĹĶĶÕ‘ďÖ^”ÚŌÚ ‹Čļā»Ói≤Ņ ’Ņs£¨◊ÓīůőĽ“∆‘Ųľ”£¨Ķęň…Ŕ|Ļ«÷≤»Ž≤ŅőĽĶ◊≤ŅĶńőĽ“∆ŽS÷Ý∑N÷≤ůwŹó–‘ń£ŃŅĶńĹĶĶÕ∂Ýúp–°£¨3#°Ę4#∑N÷≤ůw‘ŕň…Ŕ|Ļ«Ķ◊≤Ņģa…ķĶńőĽ“∆“—–°”ŕ7.5×10-3mm£®ąD11b1–11b4£©°£1#ń£–Õ∑N÷≤ůw‘ŕň…Ŕ|Ļ«É»ģa…ķĶńMisesϙѶÖ^÷ų“™ « ‹Čļā»ļÕ ‹ņ≠ā»Ō¬≤Ņ∑÷£¨Ō¬∂ň¬›ľyļÕĶ◊≤ŅϙѶ›^īů£ĽģĒ∑N÷≤ůw≤ńŃŌŹó–‘ń£ŃŅúp–°ĶĹ30GPa£®4#£©ēr£¨Ď™Ń¶Ö^÷ų“™őĽ”ŕň…Ŕ|Ļ«…Ōā»£¨Ō¬∂ň¬›ľyļÕĶ◊≤ŅϙѶ›^–°£Ľ¬›ľyťgĶńϙѶ∑÷≤ľ”…ŹńĶ◊≤ŅŌÚŪĒ≤Ņúp–°◊É읏ńĶ◊≤ŅŌÚŪĒ≤Ņ‘Ųľ”°£1#°Ę2#°Ę3#°Ę4#∑N÷≤ůw÷≤»ŽőĽ÷√…ŌŌ¬É…∂ňň…Ŕ|Ļ«ĶńϙѶ≤Óľsěť2°Ę3.5°Ę3.5°Ę5.8MPa£¨÷≤»ŽőĽ÷√Ķŕ“Ľ¬›ľyÉ…ā»Ķńň…Ŕ|Ļ«Ď™Ń¶≤Óľsěť2°Ę1.5°Ę1.5°Ę1MPa£¨‘ŕłųĹMń£–Õ÷–£¨2#Ňc3#ń£–ÕĶń∑N÷≤ůw‘ŕň…Ŕ|Ļ«÷–ģa…ķłŁĺýĄÚĶń’ŻůwϙѶ∑÷≤ľ£®ąD11c1~11c4£©°£
4°Ę”Ď’ďŇc∑÷őŲ
Īĺ—–ĺŅ≤…”√”–Ōř‘™∑Ĺ∑®—–ĺŅŃňTi6Al4VļÕ–¬–Õ…ķőÔŠt”√šÜļŌĹū”√◊ų“ĽľĢ Ĺ∑N÷≤ůwľįŌŗĎ™Ļ«ĹMŅóĶńϙѶ†ÓĎB£¨“‘‘uĻņšÜļŌĹū”√◊ų—ņŅ∆÷≤»Ž≤ńŃŌĶńĎ™”√ĚďѶ°£łýďĢ≤ńŃŌѶĆW£¨∑N÷≤ŃxżXŅ…ļÜĽĮěťÜő∂ňĻŐ∂®ĶńĎ“ĪŘŃļ£¨∆š÷–Ļ«ĹMŅóĹo”Ť∆šĻŐ∂®Ķńľs ÝѶ°£∆š◊‘”…∂ň ©ľ”ĶńôMŌÚ›dļ…∑÷ŃŅ Ļ∆šĻŐ∂®∂ňďŪ”–◊ÓīůĶńŹĚĺō°£ľÉŹĚ«ķĶń“ĽĺSĶ»Ĺō√śŃļĶńĄā∂»ěť£ļ
k=EA/L£®12£©
∆š÷–£¨E읏ó–‘ń£ŃŅ£¨AļÕL∑÷Ąe «ŃļĶńĹō√ś∑eļÕťL∂»°£
é◊ļőń£–ÕŌŗÕ¨ĶńólľĢŌ¬£¨∑N÷≤ůwŹó–‘ń£ŃŅƶ∆š…ķőÔѶĆWĶń”įŪĎĪĺŔ|…Ō“≤ «Ć¶∆šĄā∂»Ķń”įŪĎ°£Ąā∂»∑ī”≥ŃňėčľĢĶ÷ŅĻŹó–‘◊É–őĶńń‹Ń¶£¨ «Ń¶-őĽ“∆«ķĺÄĶń–Ī¬ °£Ļ ∂Ý£¨›^ĶÕń£ŃŅĶń∑N÷≤ůw◊‘”…∂ňĶńőĽ“∆›^īů£¨łŖőĽ“∆Ö^ŌÚ∑N÷≤ůwÓi≤ŅĒUīů£¨ŖM“Ľ≤Ĺ ĻĶ√Źó–‘ń£ŃŅ›^ĶÕĶń≤ńŃŌ‘ŕÓi≤Ņ◊É–ő›^īů£¨Źń∂Ý‘ŕÓi≤Ņľį÷‹áķĻ«ĹMŅó÷–ģa…ķ›^łŖĶńϙѶ£¨≤Ę«“∆§Ŕ|Ļ«≥–ďķŃňĻ«ĹMŅó÷–ĶńĹ^īů≤Ņ∑÷ϙѶ£¨Ŗ@“Ľ¨FŌůŇcīů∂ŗĒĶőńęIŌŗň∆[18,36‒38]°£Ŗ@“≤ «∂ŗĒĶ—–ĺŅĆ£◊Ę”ŕ∑N÷≤ůwľį∆š≤ŅľĢé◊ļőĹYėčĶń‘≠“Ú°£»Ű“™łń…∆ĶÕń£ŃŅ≤ńŃŌĶńŅĻ◊É–őń‹Ń¶£¨‘Ųīů∆š÷ĪŹĹ «“Ľ∑N––÷ģ”––ßĶń∑Ĺ∑®£¨”»∆š «Ňc∆§Ŕ|Ļ«Ĺ””|ĶńőĽ÷√°£Ć¶”ŕ∑N÷≤ůwĶńϙѶľĮ÷–≤ŅőĽ£¨ďĢ∆šňŻ—–ĺŅąůĶņ£¨›^ěť≥£”√ĶńÉ…∂ő Ĺ∑N÷≤—ņĶńϙѶľĮ÷–őĽ÷√Õ¨ė”ěť∑N÷≤ůwĶńÓi≤Ņ[35‒41]°£īňÕ‚£¨ůwÕ‚ĆćÚěĪŪ√ų£¨≤Ľ’ď «“Ľ∂ő ĹŖÄ «É…∂ő Ĺ∑N÷≤ůw£¨ĒŗŃ—ĺýįl…ķ‘ŕ∑N÷≤ůwĶńÓi≤ŅÖ^”Ú[42‒43]°£”…īňŅ…“‘Õ∆Ēŗ∑N÷≤ůwÓi≤ŅĶńϙѶľĮ÷– «”…∆šĎ“ĪŘŃļĶńĹYėčŐō–‘ňýõQ∂®Ķń£¨“≤ «∑N÷≤ůw ß–ßĶńÍPśIőĽ÷√°£
łýďĢTrettoĶ»[37]ƶ‚ĀŐśīķ≤ńŃŌ”√◊ų“Ľ∂ő ĹļÕÉ…∂ő Ĺ∑N÷≤—ņĶń…ķőÔѶĆW––ěťŌŗÍP—–ĺŅ£¨ĆĘŹó–‘ń£ŃŅĶÕ”ŕ∑N÷≤ůwĶń≤ńŃŌ”√◊ųĽýŇ_ĆĘēĢīŔŖMѶŌÚ∑N÷≤ůwĶńāųŖf£¨‘ŕŌŗÕ¨Ķń‚ĀĽýŇ_Ō¬£¨É…ľĢ Ĺ∑N÷≤ůwĶńϙѶ“™–°”ŕ“ĽľĢ Ĺ°£“Úīň£¨Īĺ—–ĺŅ≤…”√Ķń“Ľ∂ő Ĺ∑N÷≤ůwń£–ÕĶ√ĶĹĶńϙѶ“™łŖ”ŕ Ļ”√‚ĀĽýŇ_Ķń«ťõr£¨‘uĻņĹYĻŻŌŗƶ›^ěťĪ£ ō°£
‘ŕ∑N÷≤ůwĶńϙѶ†ÓĎB∑÷őŲ÷–Ņ…“‘ŅīĶĹ£¨4∑N≤ńŃŌĶń∑N÷≤ůwϙѶľĮ÷–ĺýőĽ”ŕÓi≤ŅŇc∆§Ŕ|Ļ«…ŌĪŪ√śŖÖĺČĹ””|ĶńĶō∑Ĺ£¨Ŗ@Ņ…ń‹ «“Úěťń£–Õ÷– Ļ”√ĶńĹČ∂®ľs ÝŌř÷∆ŃňĻ«ĹMŅóļÕ∑N÷≤ůw÷ģťgĶńŌŗƶŖ\Ą”£¨Ös≤Ľ”įŪĎ∑N÷≤ůw…Ō∂ňőīľs Ý≤Ņ∑÷Ķń◊É–ő°£ŌŗĪ»”ŕÕ¨ė”īů–°ĶńīĻ÷Ī›dļ…£¨ÉA–Ī›dļ…◊ų”√Ō¬Źó–‘ń£ŃŅ›^ĶÕĶń∑N÷≤ůwłŁ“◊ģa…ķ›^īůĶńϙѶ°£
KorabiĶ»[44]Žm»Ľ Ļ”√Ńň‘ ‘SĹ””|√śŌŗƶĽ¨Ą”Ķńń¶≤ŃĹ””|£¨Ķę∆šĹYĻŻĪŪ√ųŹó–‘ń£ŃŅ›^ĶÕĶń≤ńŃŌ≥–›dń‹Ń¶»‘»Ľ›^≤Ó£Ľ‘ŕôMŌÚ›dļ…Ķń◊ų”√Ō¬£¨ŌŗĪ»”ŕ‚ĀľįłŁłŖń£ŃŅĶń≤ńŃŌłŁ“◊įl…ķ∆∆Čń£¨īĻ÷Ī›dļ…Ō¬Ķń≥–›dń‹Ń¶≤Ę≤Ľ ‹∑N÷≤ůwŹó–‘ń£ŃŅĶńÔ@÷Ý”įŪĎ°£»Ľ∂Ý£¨‘ŕ“ĽāÄĺ◊Ĺņ÷‹∆ŕ÷–£¨∑N÷≤ŃxżX–Ť“™≥– ‹ŌŗģĒ“Ľ≤Ņ∑÷ērťgĶńÉA–Ī›dļ…£¨Ŗ@“ĽŁc‘ŕŌŗÍPĶń∆£Ąŕ—–ĺŅ÷–Ķ√ĶĹ≥š∑÷ůw¨F[45‒46]°£“Úīň£¨›^ĶÕń£ŃŅĶń∑N÷≤ůw‘ŕÉA–Ī›dļ…Ō¬ĶńѶĆW–‘ń‹ « ģ∑÷÷ō“™Ķń°£Īĺ—–ĺŅĹYĻŻÔ@ ĺ4∑N∑N÷≤ůwĶń◊ÓīůMisesϙѶ≤Ęőī≥¨Ŗ^∆šėOŌřŹä∂»£¨šÜļŌĹū‘ŕĺŖ”–ĶÕ”ŕ‚ĀĶńŹó–‘ń£ŃŅĶńÕ¨ērĺŖ”–◊„ČÚĶńѶĆW–‘ń‹°£
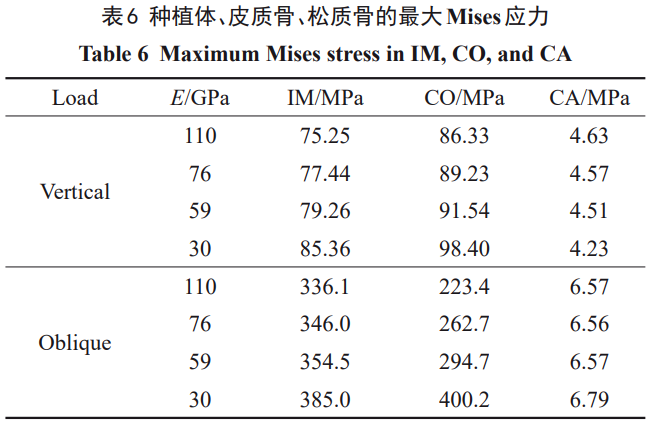
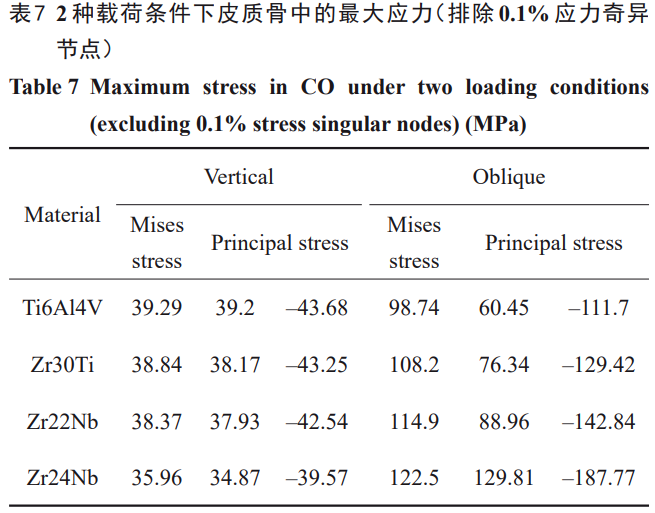
FrostĶ»»ň[47]Ľý”ŕīůŃŅŠtĆWŌŗÍPĽýĶA—–ĺŅĹ®ŃĘŃňϙѶīŐľ§ŇcĻ«ĹMŅóĶń∑īūĀ£¨ģĒ◊ų”√‘ŕĻ«ĹMŅó…ŌĶńMisesϙѶěť20~60MPaēr£¨Ď™Ń¶īŐľ§Ļ«…ķťL£ĽģĒ◊ų”√‘ŕĻ«ĹMŅó…ŌĶńMisesϙѶěť60~120MPaēr£¨Ļ«ĹMŅó“ÚŖ^›d‘ž≥…≤°ņŪ–‘Ļ«őŁ ’£Ľ≥¨Ŗ^120MPaēr£¨Ļ«ĹMŅóŅ…ń‹ēĢįl…ķĒŗŃ—°£ňý“‘ƶ÷≤»Ž≤ńŃŌĶńĎ™”√‘uĻņŖÄ–ŤįŁņ®Ļ«ĹMŅóĶńį≤»ę–‘°£»•≥ż∆śģźĻĚŁcļů£¨īĻ÷Īľ”›dŌ¬‚Ā∑N÷≤ůw‘ŕ∆§Ŕ|Ļ«ģa…ķĶńMisesϙѶľsěť39MPa£¨ÉA–Īľ”›dŌ¬ĶńMisesϙѶěť98.74MPa°£łýďĢŇRī≤—–ĺŅ£¨≥¨ōďļ… «∑N÷≤ůw÷‹áķĪŪ√śĶńŖÖĺČĻ«Ŕ|Ńų ßĶń÷ų“™‘≠“Ú÷ģ“Ľ£¨∂Ý∆§Ŕ|Ļ«“◊ ‹≥¨ōďļ…”įŪĎ£¨“ÚīňŇRī≤ŽS‘LĽľ’ŖŅŕ«Ľ÷–∑N÷≤ůwĶńĻ«Ŕ|Ńų ßť_ ľ”ŕ∆§Ŕ|Ļ«≤Ę÷ūĚuŌÚň…Ŕ|Ļ«ĒUīů£¨◊ÓĹK“żįl≤ĘįlįY”įŪĎ∑N÷≤ůwĶń∑Ä∂®–‘[48‒49]°£Õ¨ė”Ķō£¨Īĺ—–ĺŅĹYĻŻÔ@ ĺ£¨1#ń£–ÕĶń∑N÷≤ůw‘ŕ∆§Ŕ|Ļ«ēĢ‘ž≥…≤°ņŪ–‘Ļ«őŁ ’£¨Ŗ@ŇcŇRī≤…Ōįl…ķĶń‚Ā∑N÷≤ůw÷‹áķĻ«ŖÖĺČīś‘ŕĻ«őŁ ’Ķń«ťõr“Ľ÷¬£¨ĶęńŅ«įĻ«őŁ ’ «≤ĽŅ…Ī‹√‚«“›pőĘĻ«őŁ ’ «Ņ…Ĺ” ‹Ķń[9,50‒51]°£īĻ÷Īľ”›dēr£¨2#°Ę3#∑N÷≤ůw‘ŕ∆§Ŕ|Ļ«ģa…ķĶń◊ÓīůMisesϙѶ∑÷Ąeěť39ļÕ38MPa£ĽÉA–Īľ”›dēr£¨◊ÓīůMisesϙѶěť108ļÕ115MPa°£»Ľ∂Ý£¨4#∑N÷≤ůw£®30GPa£©ÉA–Īľ”›dēr‘ŕ∆§Ŕ|Ļ«ģa…ķĶńϙѶěť123MPa£¨‘ďϙѶīů–°‘ŕįl…ķĒŗŃ—ĶńŖÖĺČ£®“äĪŪ7£©°£ŌŗĪ»÷ģŌ¬£¨2#£®76GPa£©ļÕ3#£®59GPa£©∑N÷≤ůw»‘‘ŕį≤»ę Ļ”√∑∂áķÉ»°£ŅľĎ]ĶĹĻ«ĹMŅóĶńīŗ–‘£¨ņ≠ϙѶ≥¨Ŗ^«Ł∑ĢŹä∂»ēĢĆß÷¬∑N÷≤ ßĒ°[52]£¨“Úīňƶ∆§Ŕ|Ļ«Ķń◊Óīůņ≠ČļϙѶ“≤ŖM––Ńň∑÷őŲ°£ŇŇ≥żĎ™Ń¶∆śģźĻĚŁcļů£¨īĻ÷Īľ”›dēr‚Ā‘ŕ∆§Ŕ|Ļ«ģa…ķĶńņ≠ČļϙѶ◊Óīů£¨∑÷Ąeěť39ļÕ–44MPa£ĽÉA–Īľ”›dēr£¨4#£®30GPa£©∑N÷≤ůw‘ŕ∆§Ŕ|Ļ«ģa…ķĶńņ≠ČļϙѶ◊Óīů£¨∑÷Ąeěť130ļÕ–188MPa£¨Õ¨ė”“—Ĺõ∑«≥£Ĺ”ĹŁĻ«ĹMŅóĶńņ≠…žļÕČļŅsŹä∂»£¨»Ľ∂Ý2#£®76GPa£©ļÕ3#£®59GPa£©‘ŕ∆§Ŕ|Ļ«ģa…ķĶń◊Óīůņ≠ČļϙѶ∑÷Ąeěť76°Ę–129ļÕ89°Ę–143MPa£¨ĺýĶÕ”ŕ∆§Ŕ|Ļ«ĶńŹä∂»£®ŅĻņ≠Źä∂»ěť130MPa£¨ČļŅsŹä∂»ěť190MPa[18]£©£®“äĪŪ6£©°£ŹńMisesϙѶļÕ÷ųϙѶ2∑NϙѶ‘uĻņĹYĻŻŅī£¨2#£®76GPa£©ļÕ3#£®59GPa£©∑N÷≤ůwĺŖ”–Ńľļ√Ķń Ļ”√į≤»ę–‘°£ĪMĻ‹»Áīň£¨–Ť“™Źä’{Ķń «∑N÷≤ůw›^ĶÕĶńŹó–‘ń£ŃŅ‘ŕÉA–Īľ”›dērēĢ“ż∆ūϙѶĶń‘Ųľ”£¨ ĻĶ√∑N÷≤ůwÓi≤Ņľį÷‹áķ∆§Ŕ|Ļ«ĶńŖ^›dÔLŽU‘Ųľ”°£
ńŅ«į£¨—ņŅ∆÷≤»ŽőÔĶń—–ĺŅ÷¬Ń¶”ŕúp»ű“ϙѶ∆ŃĪő”–ßĎ™Ķń”įŪĎ£¨ľī∆ŕÕŻĻ«ĹMŅó ‹ĶĹłŁ∂ŗĶńϙѶīŐľ§£¨Ćć¨FłŁļ√ĶńĻ«ĹYļŌ°£ņŪŌŽĶń∑N÷≤ůw≤ńŃŌĎ™ģĒĆć¨FŃľļ√Ķń›dļ…āųŖf£¨úp–°∑N÷≤ůw-Ļ«ĹÁ√śĎ™Ń¶≤Ó[14]°£‘ŕÉ…∑Nľ”›d∑ĹŌÚŌ¬£¨ŽS÷ÝŹó–‘ń£ŃŅĶńĹĶĶÕ£¨∆§Ŕ|Ļ«…Ō∂ňĶńϙѶľĮ÷–ľį◊ÓīůϙѶ÷Ķ‘Ųľ”£¨∂ÝĶ◊≤ŅĶńϙѶ◊ÉĽĮ«ťõrĄtŌŗ∑ī°£PiotrowskiĶ»[22]ƶZr24Nb‘ŕīĻ÷Ī›dļ…Ō¬Ķń”–Ōř‘™…ķőÔѶĆWń£ĒM÷–≥Ų¨FŃňŇcĪĺ—–ĺŅŌŗÕ¨Ķń¨FŌů£¨Ķę∆§Ŕ|Ļ«ĹÁ√ś…Ō∂ň≤Ęőī≥Ų¨FϙѶľĮ÷–°£Ŗ@ «”…”ŕPiotrowskiĶ»Ķńé◊ļőń£–Õ÷–∑N÷≤ůw÷≤»ŽĻ«ĹMŅóĶńőĽ÷√›^…Ó£¨∑N÷≤ůwÓi≤ŅÕÍ»ęőĽ”ŕĻ«ĹMŅó÷–£¨∆§Ŕ|Ļ«…Ō∂ňļÕ∑N÷≤ůwĶńĹ””|√ś∑e›^īů£¨Ąā∂»“≤łŁīů°£
»Ľ∂Ý£¨∆§Ŕ|Ļ«Ķ◊≤ŅϙѶ∑÷≤ľĶńłń…∆ĪĺŔ|…Ō»‘Ňc≤ńŃŌŹó–‘ń£ŃŅŌŗÍP°£‘ŕŌŗÕ¨Ķń›dļ…ólľĢŌ¬£¨›^“»Š‹õ”ĶńĶÕń£ŃŅ≤ńŃŌłŁ“◊įl…ķ◊É–ő£¨“Úīň‘ŕ∆§Ŕ|Ļ«Ķ◊≤ŅĶńé◊ļő≤ĽŖBņmŐéģa…ķłŁīůĶń◊É–ő£¨ŃŪ“Ľ∑Ĺ√ś£¨∑N÷≤ůwļÕĻ«ĹMŅóĶńń£ŃŅ≤Óúp–°£¨◊É–őłŁěťÖf’{£¨ĹÁ√śÉ…ā»ĶńĎ™◊É≤ÓłŁ–°°ĘĎ™◊ÉÖ^∑÷≤ľŌŗƶłŁěťĺýĄÚ°£īňÕ‚£¨≤ńŃŌ≤īň…Ī»ŌŗÕ¨Ķń«ťõrŌ¬£¨›^ĶÕń£ŃŅ∑N÷≤ůw‘ŕŇc∆§Ŕ|Ļ«…Ō∂ňĹ””|őĽ÷√É»≤ŅĶń›^īůĎ™◊É—ōôMŌÚ∑÷≤ľ°£Ŗ@ «”…”ŕ∑N÷≤ůwįl…ķŃňČļŅs◊É–ő£¨īĻ÷Ī›dļ…Ō¬É»≤ŅĎ™◊ÉÖ^ŌÚŌ¬ĒUīů£¨ôMŌÚ›dļ…∑÷ŃŅŌ¬ĪŪ¨Fěť√ųÔ@ĶńĎ™◊ÉôMŌÚĒUīů£¨Źń∂ÝīŔ Ļ∑N÷≤ůw‘ŕ∆§Ŕ|Ļ«Ö^”ÚÉ»Ķń’ŻůwĎ™◊É‘Ųľ”£¨”–ņŻ”ŕϙѶŌÚ∆§Ŕ|Ļ«ĶńāųŖf°£”…”ŕ◊É–őÖf’{–‘‘Ųľ”£¨∆§Ŕ|Ļ«ĹÁ√ś…Ō∆ĹĺýϙѶ‘Ųľ”ĶńÕ¨ēr∑N÷≤ůwĶń∆ĹĺýϙѶúp–°£¨ŖM∂ÝĹÁ√śĶńϙѶ≤Ó∑«ĺÄ–‘úp–°°£“‘1#∑N÷≤ůw◊ųěťėňú £¨ÉA–Ī›dļ…Ō¬Ć¶”ŕ∑N÷≤ůw◊ÓīůMisesϙѶ£¨2#°Ę3#°Ę4#∑N÷≤ůwĶńϙѶ‘Ų∑ý∑÷Ąeěť2.98%°Ę5.47%°Ę14.55%£¨Ķę◊ÓīůϙѶ»‘–°”ŕ∆šŹä∂»£®∑÷Ąeěť952°Ę611°Ę800MPa£©£®“äĪŪ2£©£ĽĆ¶”ŕĹÁ√ś∑N÷≤ůwĶń∆ĹĺýMisesϙѶ£¨ŌŗĎ™ĶńϙѶĹĶĶÕ∑ý∂»∑÷Ąeěť8.85%°Ę15.33%°Ę32.90%£ĽĆ¶”ŕĹÁ√ś∆§Ŕ|Ļ«Ķń∆ĹĺýMisesϙѶ£¨ŌŗĎ™ĶńϙѶ‘Ų∑ý∑÷Ąeěť12.75%°Ę122.94%°Ę155.11%£¨∆š◊ÓīůϙѶ‘Ų∑ý∑÷Ąeěť17.59%°Ę31.92%°Ę79.14%£ĽĆ¶”ŕĹÁ√śĶńϙѶ≤Ó£¨ŌŗĎ™ĶńϙѶĹĶĶÕ∑ý∂»∑÷Ąeěť16.82%°Ę29.45%°Ę65.41%£®“äĪŪ8£©°£”…īňŅ…“äĹĶĶÕŹó–‘ń£ŃŅƶ”ŕīŔŖMϙѶŌÚĻ«ĹMŅóĶńāųŖf–ßĻŻ∑«≥£√ųÔ@°£Žm»Ľ∑N÷≤ůwĶńϙѶ‘Ųľ”∑ý∂»›^–°£¨Ķę≤ńŃŌĶńŹä∂»ŖÄ «“ĽāÄ÷ō“™ĶńŇ–Ēŗėňú £¨∆š÷–2#ļÕ3#∑N÷≤ůw“‘›^–°Ķń∑N÷≤ůwϙѶ‘Ų∑ýę@Ķ√›^īůĶńĹÁ√śĎ™Ń¶≤Óúp∑ý°£–Ť“™Źä’{Ķń «£¨Ŗ@∑N∑«ĺÄ–‘ŐōŁcÉHŌř”ŕĽýŇ_ļÕ∑N÷≤ůwŌŗŖBĶń“Ľ∂ő Ĺ∑N÷≤ůw°£”……Ō Ų”Ď’ďŅ…÷™£¨Ňc∑N÷≤ůwń£ŃŅŌŗÕ¨ĶńĽýŇ_ŌŗĪ»£¨łŁłŖń£ŃŅĶńĽýŇ_ēĢ Ļ∑N÷≤ůwľį÷‹áķĻ«ĶńϙѶłŁłŖ°£»Ľ∂Ý£¨ĹYļŌ∑N÷≤ůwŹó–‘ń£ŃŅƶ∆šĪĺ…Ū≥–›dń‹Ń¶Ķń”įŪĎŐō–‘£¨∑N÷≤ůwĎ™‘ŕĚM◊„∆šĆ¶ĺ◊Ĺņōď›d–Ť«ůĶń«įŐŠŌ¬ŖmģĒĹĶĶÕ∆šŹó–‘ń£ŃŅ“‘Ćć¨FłŁļ√…ķőÔѶĆW–‘ń‹£¨Ŗ@ŇcÖő‘ĹĶ»[53]”^Łc“Ľ÷¬°£∂Ý2#ļÕ3#∑N÷≤ůwń‹ČÚĚM◊„Ŗ@“Ľ“™«ů£¨≤Ę«“ƶ”ŕ∆§Ŕ|Ļ«ĺŖ”–Ńľļ√Ķń Ļ”√į≤»ę–‘°£īňÕ‚£¨»Ű“™łń…∆∆§Ŕ|Ļ«…Ō∂ňϙѶŽSŹó–‘ń£ŃŅĹĶĶÕ∂Ý‘Ųľ”Ķń¨FŌů£¨‘ŕ÷≤»ŽĻ«ĹMŅóērŖmģĒ‘Ųľ”÷≤»Ž…Ó∂» «“Ľ∑N∑Ĺ∑®°£
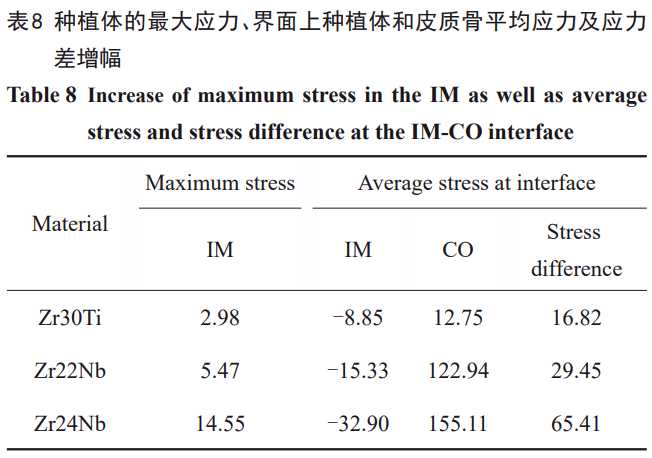
ÉA–ĪólľĢŌ¬£¨Źó–‘ń£ŃŅěť30GPaĶń4#∑N÷≤ůw‘ŕň…Ŕ|Ļ«÷≤»ŽőĽ÷√Ķ◊≤ŅĶńϙѶľĮ÷–ŌŻ ߣ¨ŇcKorabiĶ»[44]”^≤žĶž۫–Ď™◊É√ųÔ@úp»űĶń÷≤»ŽőÔń£ŃŅ£®23GPa£©Ōŗň∆°£ģĒôMŌÚ›dļ…∑÷ŃŅīś‘ŕēr£¨Źó–‘ń£ŃŅĹĶĶÕ£¨∑N÷≤ůwĶń◊É–őŌÚÓi≤ŅľĮ÷–°ĘĶ◊≤ŅĶń◊É–őúp–°£¨ňý“‘Zr24Nb‘ŕň…Ŕ|Ļ«ĶńϙѶļń…ĘľĮ÷–”ŕ÷≤»ŽőĽ÷√Ķń…Ō≤Ņ°£»Ľ∂Ý£¨‚Ā∑N÷≤ůwĄtŌŗ∑ī£¨«“‘ŕň…Ŕ|Ļ«Ķ◊≤Ņīś‘ŕ›^ěť√ųÔ@ĶńϙѶľĮ÷–°£PrimoradianĶ»[54]ņŻ”√Źó–‘ń£ŃŅŇcň…Ŕ|Ļ«ŌŗĹŁĶń”–ôC≤£Ńß≤ĘÕ®Ŗ^Ļ‚Źó–‘‘áÚěę@Ķ√ŃňÉA–Īľ”›dēršď÷≤»ŽőÔ£®190~210MPa£©‘ŕ”–ôC≤£Ńß÷–ĶńϙѶ∑÷≤ľ£¨ĹYĻŻÔ@ ĺϙѶľĮ÷–‘ŕ÷≤»ŽőĽ÷√…Ō≤ŅĶń“Ľā»ļÕĶ◊≤Ņ£¨≤Ę«“‚Ā÷≤»ŽőÔĶń”–Ōř‘™ĹYĻŻÔ@ ĺťL∂»ěť10mmĶń∑N÷≤ůw£®≤ĽÕ¨¬›ĺŗ£©‘ŕň…Ŕ|Ļ«É»ģa…ķĶń◊ÓīůϙѶěť7~8MPa£¨ĆćÚěŇcń£ĒM—–ĺŅĺýŇcĪĺ—–ĺŅĹYĻŻ›^ěť“Ľ÷¬°£
ZhangĶ»[55]ƶ∑N÷≤ůwĻ«É»∂őĶń÷–ťg≤Ņ∑÷Ď™”√ŃňĶÕĄā∂»Ķń∂ŗŅ◊ĹYėč£¨ŖM∂Ýę@Ķ√ŃňŌŗĪ»ĻŐůw‚Ā∑N÷≤ůwłŁĺýĄÚĶńϙѶ∑÷≤ľ“‘ľįłŁ–°ĶńϙѶ°£Ŗ@∑N∑Ĺ∑®ĆćŽH…Ō «‘ŕ›^łŖļÕ›^ĶÕń£ŃŅ∑N÷≤ůwƶň…Ŕ|Ļ«ģa…ķĶń2∑NϙѶŪĎĎ™ťg»°Ķ√∆Ĺļ‚°£
Ōŗň∆Ķō£¨2#°Ę3#∑N÷≤ůwĶńĄā∂»Ĺť”ŕ1#ļÕ4#∑N÷≤ůw£¨“Úīň‘ŕň…Ŕ|Ļ«÷–ģa…ķĶńϙѶ∑÷≤ľ«ťõrĄtĹť”ŕÉ…’Ŗ÷ģťg£¨÷≤»ŽőĽ÷√ĹÁ√śĶń…Ō≤ŅļÕŌ¬≤Ņõ]”–√ųÔ@ĶńϙѶ≤Óĺŗ£¨‘ŕ÷≤»ŽőĽ÷√Ķń÷‹áķĺý”–ϙѶ∑÷≤ľ£¨¬›ľyťgĶńϙѶ∑÷≤ľÖ^”Úīů–°ŌŗĹŁ£¨õ]”–≥Ų¨F«įÉ…’Ŗ¬›ľyťgϙѶ∑÷≤ľÖ^”Ú÷ūĚuúp–°Ķń¨FŌů£¨’ŻůwĶńϙѶ∑÷≤ľłŁěťĺýĄÚ°£2#°Ę3#∑N÷≤ůwģa…ķĺýĄÚĶńϙѶļń…Ęƶ”ŕň…Ŕ|Ļ« «”–ņŻĶń°£īňÕ‚£¨ÉA–Ī›dļ…Ō¬Ď™Ń¶∑÷≤ľłŁĺýĄÚĶń2#∑N÷≤ůw‘ŕň…Ŕ|Ļ«ŪĒ∂ňϙѶľĮ÷–Őéģa…ķĶńMisesϙѶ◊Ó–°°£
5°ĘĹY’ď
1£©Ć¶”ŕ“Ľ∂ő Ĺ∑N÷≤ůw£¨Źó–‘ń£ŃŅ›^ĶÕĶń∑N÷≤ůw‘ŕÉA–Ī›dļ…Ō¬Ķń≥–›dń‹Ń¶√ųÔ@úp»ű£¨‘ŕĻ«ĹMŅó÷–ģa…ķĶńϙѶłŁīů°£ĶęZr30TiļÕZr22Nb∑N÷≤ůwľįĻ«ĹMŅó÷–Ķń◊ÓīůϙѶ»‘–°”ŕ∆šŹä∂»£¨≥–›d›^īůĶń∆§Ŕ|Ļ«“≤ĺŖ”–Ńľļ√ĶńĎ™”√į≤»ę–‘°£
2£©ŽS÷ÝŹó–‘ń£ŃŅĶńĹĶĶÕ£¨“Ľ∂ő Ĺ∑N÷≤ůwÓi≤ŅÉ»≤ŅĶńĎ™◊ÉÖ^ĒUīů£¨◊É–őÖf’{–‘‘Ųľ”£¨É…’ŖĻ≤Õ¨īŔŖMŃň∑N÷≤ůwŌÚ∆§Ŕ|Ļ«ĶńϙѶāųŖf£¨úp–°Ńň∑N÷≤ůw-Ļ«ĹMŅóĶńĹÁ√śĎ™Ń¶≤Ó°£
3£©∑N÷≤ůwŹó–‘ń£ŃŅĶńĹĶĶÕīŔ Ļň…Ŕ|Ļ«÷–ĶńϙѶŌÚ…Ō≤ŅľĮ÷–£¨÷–Ķ»Źó–‘ń£ŃŅĶń≤ńŃŌ£®Zr30TiļÕZr22Nb£©‘ŕň…Ŕ|Ļ«÷–ģa…ķĶńϙѶ∑÷≤ľłŁĺýĄÚ°£
ÖĘŅľőńęI References
[1] Niinomi M, Nakai M, Hieda J. Acta Biomaterialia[J], 2012, 8(11): 3888
[2] Sato E, Shigemitsu R, Mito T et al. Computers in Biology and Medicine[J], 2021, 129: 104173
[3] Geetha M, Singh A K, Asokamani R et al. Prog Mater Sci[J],2009, 54: 397
[4] Wang Shengnan(ÕűĄŔŽy), Cui Yue(īř ‹S), Yuan Zhishan(‘¨÷ĺ…Ĺ) et al. Rare Metal Materials and Engineering(Ō°”–ĹūĆŔ≤ńŃŌŇcĻ§≥Ő)[J], 2015, 44(2): 509
[5] Sun Chunchun(ĆOľÉľÉ), Guo Zhijun(Ļý÷ĺĺż), Zhang Jinyong(ŹąĹū”¬) et al. Rare Metal Materials and Engineering(Ō°”–ĹūĆŔ≤ńŃŌŇcĻ§≥Ő)[J], 2022, 51(3): 1111
[6] Mehjabeen A, Song T, Xu W et al. Advanced Engineering Materials[J], 2018, 20(9): 1800207
[7] Luo Cong(Ń_ ¬Ē). Research on Preparation, Microstructure and Mechanical Properties of New Biomedical Zirconium Alloy[D]. Nanjing: Southeast University, 2024
[8] Liu Yangyang(ĄĘóÓóÓ). Investigation on Mechanical Properties and Bio-corrosion Resistance of Zr-2.5Nb Alloy Processed by Laser Shock Peening(ľ§Ļ‚õ_ďŰZr2.5NbļŌĹūĶńѶĆW–‘ń‹ľį…ķőÔńÕłĮőg–‘ń‹Ķń—–ĺŅ)[D]. Shenyang: Northeastern University, 2021[9] Jiang J, Zhou C, Zhao Y W et al. Journal of the Mechanical Behavior of Biomedical Materials[J], 2020, 112: 104048
[10] Hsu H C, Wu S C, Sung Y C et al. Journal of Alloys & Compounds[J], 2009, 488(1): 279
[11] Zhou Yunkai, Jing Ran, Ma Mingzhen et al. Chinese Physics Letters[J], 2013, 30(11): 3
[12] Kondo R, N mura N, Suyalatu et al. Acta Biomaterialia[J], 2011, 7(12): 4278
[13] Calì M, Zanetti E M, Oliveri S M et al. Dental Materials[J], 2018, 34(3): 460
[14] Jiang X Y, Yao Y T, Tang W M et al. Journal of Biomedical Materials Research Part A[J], 2020, 108(8): 1634
[15] Matsuzaki M, Ayukawa Y, Sakai N et al. Computer Methods in Biomechanics & Biomedical Engineering[J], 2018, 20(4): 393
[16] Bataineh K, Al Janaideh M. Clin Implant Dent Relat Res[J], 2019, 21(6): 1206
[17] Jiang Songji(Ĺ≠Š¬ůK), Wu Yin(Ö« “Ű), Si Wenjie(ňĺőńĹ›). Rare Metal Materials and Engineering(Ō°”–ĹūĆŔ≤ńŃŌŇcĻ§≥Ő)[J], 2015, 44(S1): 387
[18] Fabris D, Moura J P A, Fredel M C et al. Journal of Biomedical Materials Research Part B: Applied Biomaterials[J], 2022, 110(1): 79
[19] Lopez C A V, Vasco M A A, Ruales E et al. Journal of Oral Implantology[J], 2018, 44(6): 409
[20] Vadiraj B, Rao P K, Kiran K K. Materials Today: Proceedings[J], 2023, 76: 564
[21] Li Hongbo(ņÓÝô≤®), Yao Yueling(“¶‘¬ŃŠ). Chinese Journal of Prosthodontics(Ņŕ«ĽÓM√ś–řŹÕĆWŽs÷ĺ)[J], 2007, 8(3): 164
[22] Piotrowski B, Baptista A A, Patoor E et al. Materials Science and Engineering C[J], 2014, 38: 151
[23] Wang Rong(Õű »ō). Mechanical Behavior of Dental Implant in Mandible and New Load-transfer Method by 3D FEA(Ō¬ÓM—ņ∑N÷≤ůwѶĆW––ěťľį 3D FEA –¬–Õ›dļ…āųŖf∑Ĺ ĹĶń”–Ōř‘™∑÷ őŲ)[D]. Chengdu: Sichuan University, 2005
[24] Huang Jia(ŁS ľ—), Zheng Yang(ŗć ēD), Song Xiaomeng(ňőē‘√») et al. Stomatology(Ņŕ«ĽŠtĆW)[J], 2020, 40(5): 5
[25] Eijden T M V. Critical Reviews in Oral Biology & Medicine[J], 2000, 11(1): 123
[26] Lin D, Li Q, Li W et al. J Mech Behav Biomed Mater[J], 2009, 2(5): 410
[28] Ding X, Liao S H, Zhu X H et al. Materials & Design[J], 2015, 84(5): 144
[29] Huang H L, Hsu J T, Fuh L J et al. Computers in Biology & Medicine[J], 2010, 40(5): 525
[30] Zhang Chengxun(Źą≥…Ą◊). Study on Efficient Meshless Method for Mechanical Analysis of Orthotropic Materials(’żĹĽłųŌÚģź–‘≤ń ŃŌ Ѷ ĆW ∑÷ őŲ Ķń łŖ –ß üo ĺW łŮ ∑® —– ĺŅ) [D]. Dalian: Dalian University of Technology, 2023
[31] Dhatrak P, Girme V, Shirsat U et al. Bio Nanoscience[J], 2019, 9: 652
[33] Ziaie B, Khalili S M R. Prosthesis[J], 2021, 3(4): 300
[34] Zhang Jianguo(ŹąĹ®áÝ), Chen Chen(Íź ≥Ņ), Hu Fengling(ļķÝPŃŠ) et al. Chinese Journal of Tissue Engineering Research(÷–áÝĹMŅóĻ§≥Ő—–ĺŅ)[J], 2022, 26(4): 585
[35] Gao Wenbo(łŖőń≤®), Ma Zongmin(ŮR◊ŕ√Ů), Li Shuxian(ņÓ ÁčĻ) et al. Chinese Journal of Tissue Engineering Research(÷–áÝĹMŅóĻ§≥Ő—–ĺŅ)[J], 2022, 26(6): 875
[36] Prados-Privado M, Martínez-Martínez C, Gehrke S A et al. Biology[J], 2020, 9(8): 224
[37] Tretto P H W, Santos M B F D, Spazzin A O et al. Computer Methods in Biomechanics and Biomedical Engineering[J], 2020, 23(8): 372
[38] Menacho-Mendoza E, Cedamanos-Cuenca R, Díaz-Suyo A. The Saudi Dental Journal[J], 2022, 34(7): 579[39] Avağ C, Akkocaoğlu M. Journal of Stomatology, Oral and Maxillofacial Surgery[J], 2023, 124(1): 101298
[40] Qin S Q, Gao Z. Computer Methods in Biomechanics and Biomedical Engineering[J], 2023, 26(12): 1499
[41] Kumar S C, Kapoor R, Khan D. Materials Today: Proceedings[J], 2022, 56: 1143
[42] Wang K, Geng J, Jones D et al. Mater Sci Eng C Mater Biol Appl[J], 2016, 63: 164
[43] Shemtov-Yona K, Rittel D. Journal of the Mechanical Behavior of Biomedical Materials[J], 2016, 62: 1
[44] Korabi R, Shemtov-Yona K, Rittel D. Clinical Implant Dentistry & Related Research[J], 2017, 5(19): 935
[45] Yu Yang( ”Š —ů). Study on Connection Stability and Fatigue Performance of Dental Implants(—ņ∑N÷≤ůwŖBĹ”∑Ä∂®–‘ľį∆£Ąŕ–‘ń‹—–ĺŅ)[D]. Shenyang: Northeastern University, 2018
[46] Jiang Yang( Ĺ™ óÓ). Study of the Mechanical Properties of Denture and the Method of Evaluating Its Life Span(ŃxżXѶĆWŐō–‘ľį∆šČŘ√ŁĶń‘uĻņ∑Ĺ∑®—–ĺŅ)[D]. Wuxi: Jiangnan University, 2021
[47] Frost H M. Angle Orthod[J], 2004, 74(1): 3
[48] Jakub K, Barbara L, Joseph N et al. Coatings[J], 2021, 11(7): 865
[49] Tomas A, Pentti T, Luis A P et al. Clinical Implant Dentistry and Related Research[J], 2022, 24(4): 532
[50] Jimbo R, Halldin A, Janda M et al. Int J Oral MaxillofacImplants[J], 2013, 28(4): e171
[51] Kitamura E, Stegaroiu R, Nomura S et al. Journal of Oral Rehabilitation[J], 2005, 32(4): 279
[52] Alemayehu D B, Jeng Y R. Materials[J], 2021, 14(22): 6974
[53] Lv Yue( Öő ‘Ĺ), Xu Kan( –ž Ŕ©), Wang Liqiang( Õű ŃĘ Źä) et al. Journal of Medical Biomechanics(Št”√…ķőÔѶĆW)[J], 2017, 32(4): 5
[54] Pirmoradian M, Naeeni H A, Firouzbakht M et al. Comput Methods Programs Biomed[J], 2020, 187: 105258
[55] Zhang J Y, Zhang X, Chen Y et al. Materials[J], 2021, 14(22): 6918
£®◊Ę£¨‘≠őńėňÓ}£ļ–¬–ÕŠt”√šÜļŌĹūžoѶľ”›d”–Ōř‘™—–ĺŅ£©
tagėňļě:…ķőÔѶĆW,—ņŅ∆∑N÷≤ůw,≤ńŃŌŖxďŮ,”–Ōř‘™∑÷őŲ,Zr30Ti,Zr22Nb,≥–›dń‹Ń¶,Ļ«÷ōň‹



